Острая ревматическая лихорадка
Содержание страницы
1. ОПРЕДЕЛЕНИЕ
Острая ревматическая лихорадка (ОРЛ) – системное воспалительное заболевание соединительной ткани, обычно развивающееся у предрасположенных лиц (главным образом детей и подростков) через 2-4 недели после перенесения стрептококковой инфекции, вызванной β-гемолитическим стрептококком группы А (обычно ангины).
Хроническая ревматическая болезнь сердца (ХРБС) — заболевание, характеризующееся поражением клапанов сердца в виде послевоспалительного краевого фиброза клапанных створок или порока сердца (недостаточность и/или стеноз), сформировавшихся после ОРЛ.
ЭПИДЕМИОЛОГИЯ
По данным ВОЗ (1989), распространенность ОРЛ среди детей в различных регионах мира в 80-е годы составила 0,3—18,6 на 1000 школьников. Заболеваемость ревматизмом в Российской Федерации, снижавшаяся в течение последних десятилетий, в настоящее время составляет 0,2 до 0,8. (Н. Н. Кузьмина 1996). В Иркутске отмечается устойчивая динамика снижения общей заболеваемости ревматизмом с 3,0 до 2,6 чел., первичная заболеваемость ОРЛ находится на стабильном уровне и составляет 0,023-0,024 на 1000 населения (Калягин А.Н., Горяев Ю.А.).
Однако утверждать, что ревматизм полностью ликвидирован, было бы преждевременно. Об этом свидетельствуют вспышки болезни, наблюдавшиеся за последнее десятилетие в США и других странах, в том числе и в России. Данные ВОЗ свидетельствуют о высокой (от 20 до 50%) распространенности инфекций верхних дыхательных путей, вызванных стрептококком группы А, среди школьников, поэтому сохраняется возможность развития ОРЛ у предрасположенных к ней лиц в основном молодого возраста. Следовательно, проблема ОРЛ и ХРБС по–прежнему должна быть в центре внимания ученых–медиков, организаторов здравоохранения и практических врачей.
2. ЭТИОЛОГИЯ
Развитие ОРЛ тесно связано с предшествующей острой или хронической носоглоточной инфекцией, вызванной β-гемолитическим стрептококком группы А.
Однако далеко не все стрептококки группы А, инфицирующие носоглотку, могут вызвать ОРЛ. Во избежание гипердиагностики этого заболевания следует учитывать, что:
- многие случаи носоглоточных инфекций в действительности вызываются не стрептококками, а вирусами;
- стрептококковые фарингиты у школьников, сопровождающиеся повышением титра антистрептококковых антител в крови, не приводят к возникновению ОРЛ, если возбудитель не принадлежит к «ревматогенным» штаммам.
Особая роль отводится М-протеину, входящему в состав клеточной стенки стрептококка, который содержит антигенные детерминанты (эпитопы), имеющие сходство с компонентами сердечной мышцы, мозга и синовиальных оболочек. Ревматогенными считают М-5, М-6, М-18 и М-24. протеины. При этом определяется устойчивый гипериммунный ответ на различные антигены стрептококка с формированием антител – антистрептолизина-О (АСЛ-О), антистрептогиалуронидазы (АСГ), антидезоксирибонуклеазы (анти ДНК-зы В)
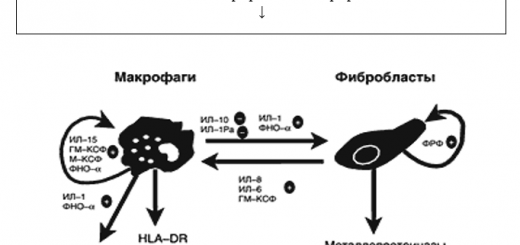
3. ПАТОГЕНЕЗ
- Наличие ревматогенных А-стрептококковых штаммов, обладающих свойствами: тропность к носоглотке, высокая контагиозность, крупные молекулы М-протеина на поверхности штаммов, наличие перекрестно-реагирующих эпитопов.
- Большая роль клеточных и гуморальных иммунных реакций: возможность участия антител к стрептолизину-О в формировании циркулирующих комплексов, стойкий высокий уровень антител к кардиолипину, увеличение концентрации интерлейкинов а1 и b1.
- Генетическая предрасположенность к заболеванию: после острой А- стрептококковай носоглоточной инфекции заболевает ОРЛ не более 0,3% лиц в популяции и до 3% в закрытых коллективах, более частая заболеваемость детей из семей, в которых кто-то из родителей страдает ревматизмом. О значении генетических факторов в определенной мере свидетельствуют результаты изучения ассоциации антигенов гистосовместимости, выявившие, частую встречаемость Dr5–Dr7, Cw2–Cw3. Генетическим маркером данного заболевания, является аллоантиген В-лимфоцитов, определяемый с помощью моноклональных антител D8/17, с большой частотой обнаруживаемый как у больных ОРЛ, так и у их ближайших родственников. С ним связывают гипериммунный ответ на стрептококковый антиген.
- За избирательное поражение клапанов сердца и миокарда с развитием иммунного асептического воспаления ответственны противострептококковые AT, перекрёстно реагирующие с тканями сердца (молекулярная мимикрия).
- Системность поражений обусловлена длительной циркуляцией формирующихся иммунных комплексов и их фиксацией в органах и тканях.
Морфологические изменения отражают системную дезорганизацию соединительной ткани, особенно сердечно-сосудистой системы со специфическими некротически-пролиферативными реакциями (гранулемы Ашоффа-Талалаева) и неспецифическими экссудативными проявлениями.
Стадии патологического процесса:
- Мукоидное набухание соединительной ткани.
- Фибриноидные изменения — необратимая стадия дезорганизации соедини тельной ткани.
- Пролиферативные реакции с образованием гранулемы Ашоффа-Талалаева.
- Фаза склероза.
4. КЛИНИЧЕСКАЯ КАРТИНА
ОРЛ характеризуется многообразием клинических проявлений и вариабельностью течения. 85- 90% пациентов, впервые заболевших ОРЛ, составляют дети и молодые люди от 3 до 20 лет. Клиническая картина развития ОРЛ у детей изменилась в последние десятилетия ХХ века:
- процентное соотношение кардита, полиартрита, хореи или их сочетаний остается достаточно постоянным,
- выраженность клинических проявлений заболевания значительно уменьшилась,
- снизилась тяжесть кардита, он протекает без отчетливых признаков недостаточности кровообращения,
- значительно уменьшилась частота серозита
- преобладает умеренная и минимальная степень активности воспалительного процесса,
- до минимума снизилась диагностическая ценность кольцевидной эритемы и ревматических узелков,
- снизилась информативность лабораторных тестов,
- значительно улучшился прогноз заболевания.
В типичных случаях первые признаки ревматизма выявляются через 2–3 нед после ангины, фарингита в виде лихорадки, симптомов интоксикации, суставного синдрома, кардита и других проявлений заболевания. Возможно, малосимптомное начало болезни с появлением утомляемости, субфебрилитета, потливость, анорексии и снижение массы тела при отсутствии заметных нарушений со стороны суставов, сердца, что может быть ошибочно расценено как остаточные явления перенесенной инфекции.
Кардит – ведущий синдром ОРЛ (90–95% случаев), который определяет тяжесть течения и исход заболевания, у 1/5 детей он протекает изолированно, а у остальных сочетается с полиартритом или хореей. К ранним симптомам относится нарушение частоты сердечных сокращений в виде тахикардии (30 — 40%) и брадикардии (20 — 39%). У 80 — 85% пациентов в дебюте заболевания отмечается умеренное расширение границ сердца. Одновременно обнаруживается ослабление тонов сердца, преимущественно первого тона, которое выявляется у подавляющего большинства больных, часто определяется дополнительный третий (40 –75%) и реже четвертый (15 — 25%) тоны.
При ОРЛ могут поражаться все три оболочки сердца — эндокард, миокард, перикард и симптоматика кардита во многом определяется поражением той или иной оболочки.
Ведущий симптом ревматического вальвулита – длительный дующий связанный с I тоном систолический шум, являющийся отражением митральной регургитации. Он занимает большую часть систолы, лучше всего прослушивается в области верхушки сердца и обычно проводится в левую подмышечную область. Митральная регургитация и дилатация сердца приводят к усилению III сердечного тона в результате быстрого сброса крови из предсердия в желудочек во время диастолы, при этом может выслушиваться за III тоном мезодиастолический шум, выслушиваемый лучше всего в положении на левом боку при задержки дыхания. Аортальный вальвулит проявляется протодиастолическим шумом в проекции аортального клапана, (аортальная регургитация). Он начинается сразу после II тона, лучше всего выслушивается вдоль левого края грудины после глубокого выдоха при наклоне больного вперед. Шум встречается нечасто в 3-5%.
При ревматическом миокардите: регистрируют дисфункцию синусового узла, миграцию водителя ритма, нарушение атрио-вентрикулярной проводимости выявляемой по ЭКГ. Перикардит при современном течении ОРЛ клинически выявляется крайне редко 1-2%, его проявления – боль, глухость сердечных тонов, нестойкий шум трения перикарда. При первой атаке ОРЛ – отмечается четкая положительная динамика под влиянием активной антиревматической терапии, происходит нормализация частоты сердечных сокращений, восстановление звучности тонов, уменьшение интенсивности систолического и диастолического шумов, сокращение границ сердца, исчезновение симптомов недостаточности кровообращения. Поражения сердца по типу миоперикардита при отсутствии вальвулита не характерно для ОРЛ и требует проведения дифференциальной диагностики с кардитами иной этиологии.
Ревматический полиартрит по-прежнему остается одним из ведущих клинических синдромов первой атаки ОРЛ. Частота его колеблется от 60 до 100%. Как правило, сочетается с кардитом и реже (10–15% случаев) протекает изолированно. Характеристика данного синдрома:
- Чаще всего поражаются крупные и средние суставы (коленные, голеностопные, локтевые, плечевые, лучезапястные), реже — тазобедренные, еще реже — мелкие суставы кистей и стоп и почти никогда — суставы позвоночника.
- При объективном исследовании обычно обнаруживают небольшую припухлость, покраснение кожи и местное повышение температуры над вовлеченными в патологический процесс суставами. Характерна диссоциация между скудными клиническими данными и резко выраженной субъективной симптоматикой — мучительными болями в пораженных суставах, особенно при движениях.
- После назначения нестероидных противовоспалительных средств (ацетилсалициловая кислота, диклофенак, ибупрофен) суставные проявления исчезают в течение нескольких дней, а нередко и часов.
- Отличительной чертой ОРЛ является «летучесть» артрита: воспалительные изменения в каком-либо одном суставе сохраняются 2–3 дня, затем появляются в другом суставе и т.д. Однако возможно одновременное поражение 2–3-х суставов и более.
- В очень редких случаях в патологический процесс вовлекается один-единственный сустав. Как правило, чем старше дети, тем меньшее число суставов поражается.
- При рентгенологическом исследовании эрозии суставных поверхностей не выявляются.
- У большинства больных ревматический полиартрит претерпевает полное обратное развитие.
Не всегда легко доказать ревматический генез сочетания изолированного полиартрита с лихорадкой и повышением острофазовых показателей (увеличение СОЭ, появление С-реактивного белка) — в силу неспецифического характера симптомов. Поскольку полиартрит чаще всего возникает в начальном периоде ревматической атаки, т. е. тогда, когда в крови титр антител к стрептококку достигает максимума, то отсутствие существенного повышения концентрации этих антител (например, АСЛ-О) является ценным предсказательным фактором, указывающим на крайне низкую вероятность ОРЛ у данного больного. С другой стороны, если титр антител повышен, то диагноз ОРЛ все равно остается предположительным. Например, повышение концентрации антител к стрептококку может быть обусловлено перенесенным недавно фарингитом. Только дальнейшее наблюдение за эволюцией артрита сможет дать ответ, является ли он симптомом ОРЛ.
В отсутствие артрита единственным признаком поражения суставов могут быть артралгии (в 10–15% случаев), интенсивность которых варьирует в широких пределах: от небольшого дискомфорта до сильных болей. В подобных случаях суставная симптоматика самопроизвольно стихает через 1–4 недели.
Необходимо помнить и о постстрептококковом реактивном артрите, который развивается после относительно короткого латентного периода, персистирует в течение более длительного времени, чем при типичной ОРЛ, и недостаточно оптимально реагирует на терапию противовоспалительными препаратами. Первоначально возник вопрос, не является ли данная нозологическая форма доброкачественно протекающим вариантом реактивного артрита, наблюдаемого после ряда бактериальных и вирусных инфекций. Однако в дальнейших исследованиях была подтверждена возможность развития повторной ОРЛ и ревматического вальвулита у пациентов, у которых первые эпизоды заболевания протекали по типу постстрептококкового артрита. Таким образом, согласно рекомендациям ВОЗ, больные с постстрептококковым реактивным артритом, формально удовлетворяющие критериям Джонса, при условии исключения артритов другого генеза должны рассматриваться как пациенты с ОРЛ со всеми вытекающими последствиями, касающимися лечения, профилактики и динамического наблюдения.
Ревматическая хорея (малая хорея, хорея Сиденгама) диагностируется в 6–30% случаев, преимущественно у детей, редко у подростков. Чаще отмечается у девочек и девушек. Хорея проявляется отрывистыми бесцельными движениями, которые становятся более выраженными при физическом напряжении, но исчезают во сне. Ребенок с хореей производит впечатление неуклюжего, гримасничающего, с нечеткой речью. Вообще, неуклюжесть, иногда — в сочетании с эмоциональной лабильностью,— наиболее характерные проявления хореи. В тяжелых случаях развивается прогрессирующая слабость. Основные клинические проявления – это пентада синдромов, наблюдающихся в различных сочетаниях:
- хореические гиперкинезы
- мышечная гипотония (вплоть до дряблости мышц с имитацией параличей)
- расстройства статики и координации
- сосудистая дистония
- психоэмоциональные нарушения (неустойчивость настроения, раздражительность, плаксивость и т.д.).
Малая хорея, как правило, сочетается с другими клиническими синдромами ОРЛ (кардит, полиартрит), однако у 5–7% больных она может быть единственным проявлением болезни. Длительность атаки ОРЛ в виде малой хореи составляет от 3 до 6 мес, однако остаточные явления могут сохраняться до 1 года. В тех редких случаях, когда хорея является единственным симптомом ОРЛ, острофазовые показатели и титры антистрептококковых антител часто возвращаются к исходному уровню. При отсутствии других критериев ОРЛ диагноз ревматической хореи правомочен только при условии исключения прочих причин поражения нервной системы (хорея Геттингтона, системная красная волчанка, болезнь Вильсона, лекарственные реакции и т.д.).
Кольцевидная (анулярная) эритема (4 – 17% случаев) характеризуется бледно-розовыми кольцевидными варьирующими в размерах высыпаниями, локализующимися, главным образом, на туловище и проксимальных отделах конечностей (но не на лице!). Она носит транзиторный мигрирующий характер, не сопровождается зудом или индурацией и бледнеет при надавливании.
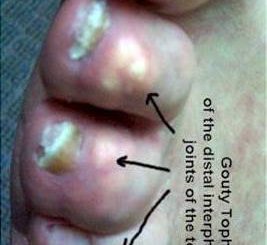
Ревматические узелки (1 – 3 %) представляют собой округлые малоподвижные безболезненные быстро возникающие и исчезающие образования различных размеров на разгибательной поверхности суставов, в области лодыжек, ахилловых сухожилий, остистых отростков позвонков, а также затылочной области hallea aponeurotica.
По мнению большинства исследователей, несмотря на значительное снижение частоты кольцевидной эритемы и ревматических узелков у детского контингента больных и фактическое отсутствие таковых у подростков и взрослых пациентов, специфичность данных синдромов для ОРЛ остается очень высокой, в силу чего они сохраняют свою диагностическую значимость и по-прежнему фигурируют в качестве “больших” критериев.
Дополнительные клинические проявления: у детей и подростков могут наблюдаться боли в животе, тахикардия без связи с повышением температуры тела, недомогание, анемия, боли за грудиной. Поскольку эти симптомы часто встречаются при многих заболеваниях, они не входят в диагностические критерии, но могут служить дополнительным подтверждением диагноза ОРЛ.
5. ДИАГНОСТИКА
Основные симптомы ОРЛ — полиартрит, кардит, хорея и, более редкие, но не менее характерные — подкожные узелки и кольцевидная эритема. В 50-х годах Т.Д.Джонс объединил эти ведущие симптомы с малыми признаками системного воспаления (лихорадка, ускоренная скорость оседания эритроцитов (СОЭ), повышение концентрации С-реактивного белка) в группу специфических критериев диагностики ОРЛ.
В таблице 1 представлена схема диагностических критериев Джонса.
Таблица 1. Диагностические критерии Джонса (АКА, 2002; АРР, 2003).
| Критерии Джонса в модификации АРР, 2003 | |||
| Большие
критерии |
Малые критерии | Данные, подтверждающие предшествовавшую А-стрептококковую инфекцию | |
| Кардит
Полиартрит Хорея Кольцевидная эритема Подкожные ревматические узелки |
Клинические | Артралгия
Лихорадка |
Позитивная А-стрептококковая культура, выделенная из зева, или положительный тест быстрого определения А- стрептококкового антигена.
Повышение или повышающие титры противострептококковых антител АСЛ-О, анти-ДНК-аза В |
| Лабораторные | Повышенные острофазовые реактанты:
СОЭ С-реактивный белок |
||
| Инструментальные | Удлинение интервала PR на ЭКГ
Признаки митральной и/или аортальной регургитации при Доплер –ЭхоКГ |
||
Примечания: Наличие двух больших критериев или одного большого и двух малых в сочетании с данными, документировано подтверждающими предшествующую инфекцию стрептококками группы А, свидетельствует о высокой вероятности ОРЛ.
Особые случаи:
- Изолированная (чистая) хорея- при исключении других причин.
- Поздний кардит- растянутое во времени (>2 мес.) развитие клинических и инструментальных симптомов вальвулита — при исключении других причин.
- Повторная ОРЛ на фоне ХРБС (или без нее).
Малые диагностические критерии Джонса рассматриваются только при условиях, что они выявляются впервые у конкретного больного и не имеют под собой других причин.
На ЭКГ при ревмокардите нередко выявляются нарушения ритма (тахи– или брадиаритмия, миграция водителя ритма, иногда экстрасистолия, фибрилляция предсердий), замедление атриовентрикулярной проводимости преимущественно I степени (РQ>0,2сек), нарушения реполяризации желудочков, удлинение электрической систолы, при вальвулите аортальных клапанов нередко регистрируются признаки диастолической перегрузки левого желудочка.
К особенностям ЭКГ подросткового возраста относятся: синусовая брадикардия, особенно у юношей, миграция водителя ритма по предсердиям, нарушение проведения возбуждения по правой ножке пучка Гиса и реполяризации желудочков в виде высоких зубцов Т в грудных отведениях.
Важным инструментальным методом, способствующим диагностике ревмокардита, является двухмерная эхокардиография (ДЭхоКГ) с использованием допплеровской техники, которая позволяет оценивать анатомическую структуру сердца, состояние внутрисердечного кровотока, а также установить наличие перикардиального выпота, можно достоверно различить ревматический вальвулит, пролапс митрального клапана и другую патологию сердца.
Ревматический вальвулит митрального клапана имеет следующие признаки:
- краевое утолщение, рыхлость, «лохматость» створок клапана;
- ограничение подвижности утолщенной задней створки;
- наличие митральной регургитации, степень которой зависит от тяжести поражения;
- небольшой концевой пролапс (2 — 4 мм) передней или задней створки.
Вальвулит аортального клапана:
- утолщение, рыхлость эхосигнала аортальных створок, чаще утолщение правой коронарной створки.
- аортальная регургитация (направление струи к передней митральной створке);
- высокочастотное трепетание передней митральной створки, вследствие аортальной регургитации.
ЭхоКГ – феномены клапанной регургитации должны быть подтверждены при повторном исследовании через 10–14 дней.
В силу высокой чувствительности данного метода в последние годы стало возможным распознавание афоничной, т.е. без аускультативных симптомов, клапанной регургитации /КР/ — феномена, достаточно сложного для однозначной интерпретации вследствие его встречаемости у здоровых лиц, в том числе среди подростков. О функциональном или «физиологическом» характере КР целесообразно судить только после комплексного ЭКГ – исследования, определения лабораторных параметров ОРЛ и повторного эхогардиографического обследования через несколько недель.
Данные, подтверждающие предшествующую А- стрептококковую носоглоточную инфекцию необходимо помнить:
- Позитивная А-стрептококковая культура, выделенная из зева больного, может быть как доказательством активной инфекции, так и отражением бессимптомного носительства данного микроба.
- Негативные результаты микробиологического исследования, как и отрицательные данные теста быстрого определения антигена, не исключают активную А-стрептококковую инфекцию.
- Диагностическая значимость исследования противострептококкового иммунитета повышается при одновременном определении нескольких типов антител (антистрептолизин-О, антистрептокиназа, антистрептогиалуронидаза, антидезоксирибонуклеаза-В).
- При вялотекущем ревмокардите или «изолированной» хорее титры противострептококковых антител могут быть нормальными.
- Повышение уровня перечисленных антител может наблюдаться после глоточных инфекций, вызванных b-гемолитическими стрептококками группы C или G, не имеющими отношения к ОРЛ.
- Более надежны серологические исследования, позволяющие выявить повышенные или (что важнее) повышающиеся титры противострептококковых антител: АСЛ-О, анти-ДНК-аза В, АСГ.
При отсутствии серологического ответа на стрептококковый антиген в сочетании с негативными микробиологическими результатами диагноз ОРЛ представляется маловероятным. Однако необходимо заметить, что уровень противострептококковых антител, как правило, повышен в раннем периоде заболевания и может снижаться или быть нормальным, если между началом ОРЛ и проведением исследования прошло несколько месяцев. Чаще всего это наблюдается у больных с ревматической хореей. Подобная закономерность встречается и у пациентов с поздним кардитом.
6. КЛАССИФИКАЦИЯ
Таблица 2. Классификация ОРЛ (АРР, 2003; с изменениями, ОССН, 2006).
| Клинические варианты | Клинические проявления | Исход | ХСН | ||
| Основные | Дополнительные | Стадии | ФК | ||
| Острая ревматическая лихорадка
Повторная ревматическая лихорадка |
Кардит
Артрит Хорея Кольцевидная эритема Подкожные ревматические узелки |
Лихорадка
Артралгии Абдоминальный синдром Серозиты |
Выздоровление
Хроническая ревматическая болезнь cердца: -без порока сердца** -с пороком сердца *** |
I ст
II A ст II Б ст III ст |
I ФК
II ФК IIIФК IV ФК |
Примечания: ** – возможно наличие поствоспалительного краевого фиброза клапанных створок без регургитации, которое уточняется с помощью ЭхоКГ;
*** – при наличии впервые выявленного порока сердца необходимо, по возможности, исключить другие причины его формирования (инфекционный эндокардит, первичный антифосфолипидный синдром, кальциноз клапанов дегенеративного генеза и др.)
В представленной классификации выделяется два варианта исходов заболевания. При выздоровлении речь идет о полном обратном развитии клинической симптоматики ОРЛ с нормализацией лабораторных показателей и отсутствием каких–либо остаточных изменений.
Под хронической ревматической болезнью сердца понимается заболевание, характеризующееся поражением сердечных клапанов в виде поствоспалительного краевого фиброза клапанных створок или порока сердца (недостаточность и/или стеноз), сформировавшегося после перенесенной ОРЛ.
ОРЛ, как проблема большой социальной значимости, определяется приобретенными РПС, которые по мере прогрессирования приводят к стойкой нетрудоспособности и преждевременной смерти. Частота формирования РПС после первой атаки ОРЛ у детей составляет 20–25%. Преобладают изолированные пороки сердца, чаще митральная недостаточность. Реже формируется недостаточность аортального клапана, митральный стеноз и митрально–аортальный порок. Примерно у 7–10% детей после перенесенного кардита формируется пролапс митрального клапана. Среди подростков, перенесших первую атаку ОРЛ, пороки сердца диагностируются в 1/3 случаев. У взрослых пациентов данный показатель составляет 39–45%, причем максимальная частота возникновения РПС (>75%) наблюдается в течение первых трех лет от начала болезни. У больных, перенесших первую атаку ОРЛ в возрасте 23 лет и старше, сочетанные и комбинированные РПС формируются в 90% случаев.
Повторная атака у больных с ревматическим анамнезом рассматривается, как новый эпизод ОРЛ, а не является рецидивом первого. В этих условиях (особенно на фоне сформированного порока сердца, когда диагностика кардита в значительной степени затруднена), на рецидив будет определенно указывать появление нового шума при аускультации сердца (свидетельство вовлечения в патологический процесс ранее непораженного клапана) либо присоединение прежде отсутствовавших признаков поражения сердца: острого перикардита, внезапного увеличения размеров сердца. Предположительный диагноз повторной ОРЛ может быть поставлен на основании одного «большого» или только «малых» критериев в сочетании с повышенными или повышающимися титрами противострептококковых антител. Окончательный диагноз возможен лишь после исключения интеркуррентного заболевания и осложнений, связанных с пороками сердца (в первую очередь, инфекционного эндокардита).
Важно отметить, что при наличии впервые выявленного порока сердца необходимо, по возможности, уточнить его генез (перенесенный инфекционный эндокардит и др.).
Хроническая сердечная недостаточность (ХСН) оценивается в соответствии с классификацией ОССН 2006.
По МКБ-10 ревматизм классифицируется следующим образом:
1.Острая ревматическая лихорадка (ОРЛ):
- І 00 Ревматическая лихорадка без вовлечения сердца (ревматический артрит).
- І 01 Ревматическая лихорадка с вовлечением сердца (ревматический эндокардит, вальвулит, перикардит, миокардит, панкардит).
- І 02 Ревматическая хорея (с вовлечением или без вовлечения сердца).
2. Хроническая ревматическая болезнь сердца (ХРБС):
- І 05 Ревматические болезни митрального клапана.
- І 06 Ревматические болезни аортального клапана.
- І 07 Ревматические болезни трехстворчатого клапана.
- І 08 Поражение нескольких клапанов.
Примеры клинического диагноза (АРР, 2003), в соответствии с рубрикацией МКБ–Х, представлены в таблице 3.
Таблица 3. Примеры клинических диагнозов.
| 1. Острая ревматическая лихорадка: кардит, митральный вальвулит, мигрирующий полиартрит, ХСН I ст, ФК I
2. Острая ревматическая лихорадка: хорея 3. Повторная ревматическая лихорадка: кардит. Сочетанный митральный порок сердца. ХСН II А ст., ФК II 4. Хроническая ревматическая болезнь сердца: поствоспалительный краевой фиброз створок митрального клапана. 5. Хроническая ревматическая болезнь сердца: комбинированный митрально- аортальный порок сердца. ХСН II Б, ФК III. |
І 01.1
І 02.9 І 01.9 І 05.9 І 08.0 — шифр по МКБ-10 |
План обследования. В настоящее время нет какого-либо одного специфического метода исследования, результаты которого позволяли бы диагностировать ОРЛ. Диагноз ставится на основании клинических данных, подтвержденных лабораторными исследованиями.
- Исследуют мазки из горла (хотя стрептококки группы А выделяются только в 15–20% случаев).
- В клиническом анализе крови нередко обнаруживают анемию и небольшой лейкоцитоз.
- Для исключения инфекционного эндокардита производят посев крови.
- Еженедельно определяют острофазовые показатели – СОЭ, СРБ. Хроническая сердечная недостаточность может маскировать увеличение СОЭ, однако тенденция к повышению СРБ, как правило, сохраняется.
- Титры антистрептококковых антител должны измеряться трижды через 2-недельные интервалы времени. Желательно определение различных противострептококковых антител: АСЛ-О, анти-ДНК-азы В, АСГ. Двукратное повышение титра может рассматриваться как диагностически значимое.
- ЭГК
- ЭхоКГ
- Консультация ревматолога
7. ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ
Наличие только одного из основных критериев (кардит, полиартрит, хорея) может привести к гипердиагностике ОРЛ. В отсутствие четкой связи между перенесенной стрептококковой инфекцией и кардитом необходимо исключить: вирусный миокардит, инфекционный миокардит.
Для вирусного миокардита характерно:
- Хронологическая связь с острой носоглоточной (чаще вирусной) инфекцией.
- Укорочение (менее 5 – 7 дней) или отсутствие латентного периода.
- Постепенное развитие заболевания.
- Отсутствие артрита и выраженных артралгий.
- Активный и эмоционально окрашенный характер кардиальных жалоб.
- Отсутствие вальвулита.
- Редкое обнаружение перикардита.
- Симптомы астенизации, нарушения терморегуляции в дебюте болезни.
- Медленная динамика под влиянием противовоспалительной терапии.
- Иммунологический анализ позволяет обнаружить в крови циркулирующие аутоантитела, характерные для вирусного миокардита или четырехкратное повышение титра антител к различным вирусам (Коксаки-70%)
Для инфекционного эндокардита характерно:
- Чаще встречается в среднем возрасте, дети болеют редко.
- Предрасполагающие факторы: ревматические пороки, оперативные вмешательства, в/в наркоманы, эндогенные источники инфекции.
- Нарастание шумов в сердце, прогрессирующая сердечная недостаточность.
- Быстрое формирование пороков сердца.
- Часто тромбоэмболический синдром.
- Duke-критерии: положительная гемокультура, характерная для ИЭ, наличие типичных ЭхоКГ признаков ИЭ.
Дифференциальный диагноз ревматического полиартрита проводится с большой группой состояний и болезней, протекающих с суставным синдромом: реактивные артриты иной этиологии -энтерогенные, урогенные, ревматоидным артритом, ювенильным идиопатическим артритом, клещевым боррелиозом.
Для реактивного артрита энтерогенной, урогенной этиологии характерно:
- Наличие хронологической связи между кишечной или мочеполовой инфекциями, подтвержденными микробиологическими и серологическими исследованиями.
- Конъюнктивит, поражения кожи и слизистых оболочек (кератодермия, ониходистрофия, баланит или баланопостит).
- Острый стойкий асимметричный артрит преимущественно суставов нижних конечностей (особенно суставов пальцев стоп), энтезопатии, пяточные бурситы.
Для ревматоидного артрита характерно:
- Поражаются чаще пястно-фаланговые, проксимальные межфаланговые суставы и суставы запястья.
- Характерен феномен утренней скованности, интенсивность и длительность которой коррелируют с активностью болезни.
- Симметричность поражения суставов.
- Рентгенологические изменения суставов, околосуставной остеопароз, образование эрозий или узур, сужение суставных щелей.
Для ювенильного идиопатического артрита характерно:
- Хроническое воспалительное заболевание суставов.
- На поздних стадиях возникают эпифизарные нарушения, сужение суставной щели и костные эрозии.
Для клещевого боррелиоза характерно:
- Возбудителем является спирохета borrelia burgdorferi, передаваемая при укусе клеща.
- Имеет значение анамнестические данные и определение антител к В. burgdorfer в крови.
- Развитие артрита, кардита, поражение ЦНС (энцефалит) и кожи (хроническая мигрирующая эритемы), которая образуется в месте укуса клеща.
- Эритема имеет вид кольца с красным ободком и бледным центром, в зоне эритемы жжение, распирание, онемение, зуд.
8. ЛЕЧЕНИЕ
Лечение ОРЛ – комплексное, складывающееся из этиотропной, противовоспалительной и симптоматической терапии, а также реабилитационных мероприятий.
Всем пациентам с ОРЛ показана госпитализация с соблюдением постельного режима в течение первых 2 – 3 нед болезни. Назначают диету, богатую витаминами и белками, с ограничением соли и углеводов.
Этиотропная терапия, направленная на эрадикацию БГСА-осуществляется препаратами пенициллинового ряда – бензилпенициллин 400 000–1 000 000 ЕД 4 раза в сутки в/м в течении 10 дней.
При аллергии к пенициллинам назначают макралиды или линкозамиды:
- Рокситромицин 150 мг 2 раза в сутки внутрь.
- Кларитромицин по 250мг 2 раза в сутки внутрь.
Исключительное значение придает антибактериальной профилактике повторных атак ОРЛ, которая начинается сразу после завершения курса этиотропной терапии и проводится бензатин бензилпенициллина в режиме вторичной профидактике (см. профилактика).
Наибольший риск повторной атаки ОРЛ отмечается впервые 3 года. Каждому рецидиву предшествует новый эпизод стрептококковой инфекции.
Патогенетическое лечение ОРЛ заключается в применении нестероидных противовоспалительных препаратов (НПВС) и глюкокортикостероидов (ГКС).
Желательно не назначать НПВС и ГКС пока диагноз ОРЛ не подтвержден.
НПВС назначают при:
- слабовыраженном ревмокардите;
- артралгиях, без признаков ревматического артрита;
- при минимальной активности процесса – лабораторные показатели СОЭ, лейкоцитоз, СРБ соответствуют норме или изменены незначительно;
- при отмене ГКС;
- при повторной ОРЛ на фоне ревматического порока сердца.
Препаратом первой линии терапии ОРЛ у взрослых рекомендуют аспирин в дозе 100 мг/кг/сут в равных дозах в 4-5 приема, до достижения клинического улучшения, доза может быть увеличена до 6-8 г/сут. Оптимальная доза аспирина должна обеспечивать хороший клинический ответ, но не быть токсичной.
После двух недель приема аспирина, доза может быть уменьшена до 60-70 мг/кг/сут и назначаться еще 3-6 недель. У 5% больных признаки активности ревматического процесса сохраняются свыше 6 месяцев, и может потребоваться более длительный курс приема НПВП.
По рекомендациям АРР 2003г препаратом первой линии терапии ОРЛ у взрослых рекомендуют Диклофенак взрослым и подросткам по 25-50 мг 3 раза в сутки, детям по 0.7-1 мг/кг 3 раза в сутки до нормализации показателей воспалительной активности, в среднем в течении 1.5- 2 месяцев.
- При ОРЛ с тяжелым кардитом (панкардитом), полисерозитами, максимальной активностью воспалительного процесса, СОЭ >30 мм/ч применяют ГКС.
Преднизолон – назначают взрослым и подросткам в суточной дозе 20 – 30 мг, детям по 0.7-0.8 мг/кг, в один прием утром после еды, до достижения терапевтического эффекта, как правило, в течение 2 нед, с последующим снижением дозы (2,5 мг каждые 5 – 7 дней) вплоть до полной отмены. Общая продолжительность курса лечения 1,5-2 мес.
При наличии симптомов недостаточности кровообращения в план лечения включают сердечные гликозиды и диуретики. Однако следует заметить, что назначение этих препаратов (в сочетании с противовоспалительными средствами) оправдано при активном течении ревматического процесса только на фоне РПС. В случаях развития сердечной декомпенсации, как следствия панкардита (что, как правило, встречается только в детском возрасте), применение кардиотонических препаратов нецелесообразно, поскольку в этих случаях явный терапевтический эффект может быть достигнут при использовании высоких доз преднизолона (40 – 60 мг в сутки). Одновременно хотелось бы предостеречь от назначения ГКС больным с РПС и застойной недостаточностью кровообращения.
9. ПРОФИЛАКТИКА
Основу первичной профилактики ОРЛ составляют своевременная диагностика и адекватная антимикробная терапия острой и хронической рецидивирующей БГСА- инфекции верхних дыхательных путей (тонзилит, фарингит). Таблица № 4
У лиц молодого возраста при фарингите, вызванном БГСА, имеющих факторы риска развития ОРЛ:
- отягощенная наследственность,
- неблагоприятные социально-бытовые условия
- вспышка инфекции БСГА в детских дошкольных учреждениях, школах, интернатах, воинских частях
показано 5-дневное лечение бензилпенициллином с последующей однократной инъекцией бензатин бензилпенициллина взрослым 2.4 млн Ед 1 раз, детям с массой тела <25 кг по 0.375г/кг в 2 прием, детям с массой тела >25 кг по 750 мг/сут в 2 приема.
В иных ситуациях возможно применение оральных пенициллинов в течение 10 дней. Предпочтение отдается амоксициллину, который по противострептококковой активности аналогичен ампициллину и феноксиметилпенициллину, но значительно превосходит их по своим фармакокинетическим характеристикам. Рекомендуемая схема применения амоксициллина – 1 – 1,5 г (для взрослых и детей старше 12 лет) и 500 – 750 мг (для детей от 5 до 12 лет) в сутки в течение 10 дней.
Таблица 4. Антибактериальная терапия острого и рецидивирующего стрептококкового тонзиллита (Страчунский Л.С. и соавт., 2002)
| Препараты | Режим дозирования (взрослые) |
Особенности применения |
| Препараты выбора | ||
| Феноксиметилпенициллин | 0,25 г каждые 8-12 ч | Внутрь, за 1 ч до еды, в течение 10 дней |
| Бензилпенициллин | 500 тыс. ЕД каждые 8-12 ч | В/м |
| Бензатин бензилпенициллин | 2,4 млн ЕД | В/м, однократно |
| Альтернативные препараты | ||
| Амоксициллин | 0,5 г каждые 8 ч | Внутрь, независимо от приема пищи, в течение 10 дней |
| Амоксициллин/ клавуланат* | 0,625 г каждые 8 ч | Внутрь, в начале еды, в течение 10 дней |
| Цефалексин | 0,5 г каждые 6 ч | Внутрь, за 1 ч до еды, в течение 10 дней |
| Цефадроксил | 0,5 г каждые 12 ч | Внутрь, независимо от приема пищи, в течение 10 дней |
| При аллергии на β-лактамные антибиотики | ||
| Эритромицин | 0,25-0,5 г каждые 6 ч | Внутрь, за 1 ч до еды, в течение 10 дней |
| Азитромицин | 0,5 г 1 раз в сутки | Внутрь, за 1 ч до еды, в течение 5 дней |
| Кларитромицин | 0,5 г каждые 12 ч | Внутрь, независимо от приема пищи, в течение 10 дней |
| Мидекамицин | 0,4 г каждые 8 ч | Внутрь, до еды, в течение 10 дней |
| Клиндамицин* | 0,15 г каждые 6 ч | Внутрь, за 1-2 ч до еды, в течение 10 дней |
*Рекомендуются для лечения рецидивирующего стрептококкового тонзилита.
Антибиотики линкозамиды (клиндамицин) назначают только при непереносимости как беталактамов, так и макролидов. Широкое применение этих препаратов при данных нозологических формах не рекомендуется во избежание утраты их роли как средств выбора для лечения инфекционной патологии костно-суставной системы.
Рецидивирующий тонзиллит, вызванный БГСА
В этой ситуации вероятность колонизации очага инфекции микроорганизмами, продуцирующими бета-лактамазы, достаточно высока, поэтому целесообразно проведение курса лечения ингибитор-защищенными пенициллинами (амоксициллин/клавуланат) или оральными цефалоспоринами II поколения (цефуроксим аксетил), а при непереносимости беталактамных антибиотиков — линкозамидами (табл. 4). Указанные антибиотики также рассматриваются как препараты второго ряда для случаев безуспешной пенициллинотерапии острых стрептококковых тонзиллитов/фарингитов (что чаще встречается при использовании феноксиметилпенициллина). Универсальной же схемы, обеспечивающей 100% элиминацию А-стрептококка из глотки, в мировой клинической практике не имеется.
Необходимо отметить, что применение тетрациклинов, сульфаниламидов, ко-тримоксазола и хлорамфеникола при А-стрептококковой инфекции глотки в настоящее время не оправдано по причине высокой частоты резистентности и, следовательно, низких показателей эффективности терапии.
10. ВТОРИЧНАЯ ПРОФИЛАКТИКА
Вторичная профилактика направлена на предупреждение повторных атак и прогрессирования заболевания у лиц, перенесших ОРЛ, и предусматривает регулярное введение пенициллина пролонгированного действия бензатин бензилпенициллина. Выпускаемая отечественной промышленностью пролонгированная лекарственная форма пенициллина – бициллин–5 на сегодняшний день не является приемлемой для проведения вторичной профилактики ОРЛ, поскольку не соответствует фармакокинетическим требованиям, предъявляемым к превентивным препаратам.
Таблица 5 Длительность вторичной профилактики (ВОЗ, 2001).
| Категории пациентов | Длительность профилактики |
| Пациенты без кардита (артрит, хорея) | не менее 5 лет после последней атаки, либо до достижения ими 18-летнего возраста. |
| Пациенты с кардитом незначительная митральная регургитация или излеченный кардит). | не менее 10 лет после последней атаки, либо до достижения ими 25-летнего возраста. |
| Пациенты с тяжелыми пороками | Всю жизнь |
| Пациенты после хирургического лечения | Всю жизнь |
Взрослым и подросткам: бензатин бензилпенициллин в/м 2,4 млн. ЕД 1раз в 3 недели.
Длительность вторичной профилактики (которую необходимо начинать еще в стационаре) для каждого пациента устанавливается индивидуально (таблица 5).
После прекращения 5-летней профилактики повторные атаки ОРЛ регистрируются, в зависимости от возраста, у 6–11% больных. Поэтому желательно увеличить минимальную длительность профилактики до 10 лет. Важно подчеркнуть, что профилактика проводится круглогодично, а не по сезонам.
ЛИТЕРАТУРА
- Белов Б.С. Острая ревматическая лихорадка: современное состояние проблемы. РМЖ.2005; 6:18
- Белов Б.С., Насонова В.А., Гришаева Т.П., и др. Острая ревматическая лихорадка и А-стрептококковый тонзиллит: современное состояние проблемы, вопросы антибиотикотерапии. Антибиотики и химиотерапия 2000;4:22-27.
- Калягин А.Н., Горяев Ю.А., Злобина Т.И. Анализ заболеваемости ревматизмом в Иркутске. Современные проблемы ревматологии: Сборник статей. Иркутск, 2002,25-28.
- Калягин А.Н., Горяев Ю.А., Казанцева Н.Ю. Стрептококковая инфекция в ревматологии. Журнал инфекционной патологии. 2004; 11:1. с. 13-21.
- Лыскина Г.А., Шишов А.Я. Ревматизм у детей: современное состояние проблемы РМЖ 2000; 8: 1.
- Насонова В.А., Насонов Е. Л.Рациональная фармакотерапия ревматических заболеваний. Москва: Издательство «Литтерра», 2003, с.70-78.
- Насонова В.А., Кузьмина И.И., Белов Б.С. Классификация и номенклатура ревматической лихорадки. НПР 2004; 2:48-51.
- Страчунский Л.С., Козлов С.Н. Практическое руководство по антиинфекционной химиотерапии. М.: Боргес, 2002, с 32-9.
- Ferrieri P, for the Jones Criteria Working Group. Proceedings of the Jones Criteria Workshop. Circulation. 2002;106:2521-2523.
- NHFA, CSANZ. Diagnosis and management of acute rheumatic fever and rheumatic heart disease in Australia. 2006.
- Rheumatic fever and rheumatic heart disease. Report of a WHO Expert Consultation Geneva, 2001 (Technical Report Series № 923).