Подагра. Причины, лечение, классификация подагры
Содержание страницы
1. Метаболизм пуринов
Производные пурина содержатся во всех клетках организма и являются важнейшими составными частями нуклеиновых кислот и нуклеотидов. Это главным образом аденин (6-аминопурин) и гуанин (2-амино-6-оксипурин) и в очень незначительных количествах метилированные прозводные аденина и гуанедина (метиладенин, диметиладенин, метил- и диметилгуанин и другие). Аминопурины являются слабыми основаниями, а у оксипуринов преобладают кислотные свойства. Пуриновые основания плохо растворимы в воде.
В процессе обмена веществ в организме аденин и гуанин окисляются соответственно в гипоксантин (6-оксипурин) и ксантин (2,6-диоксипурин).
Конечным продуктом обмена пуринов у человека и человекообразных обезъян является мочевая кислота, представляющая собой 2,6,8-триоксипурин, являющийся слабой двуосновной кислотой (рН 5,7 и 10,3)., почти не растворимой в воде. Мочевая кислота – постоянная составляющая часть мочи и крови. В сутки с мочой выделяется 0,3 – 1,2 г мочевой кислоты, в крови ее содержание составляет 2 – 4 мг%.. В плазме, внеклеточной и синовиальной жидкости она содержится главным образом в виде солей (уратов). Мочевая кислота практически не связывается с белками плазмы. При рН 7,4 мочевая кислота на 98% представлена мононатриевой солью, которая легко удаляется из плазмы при гемофильтрации.
У большинства других млекопитающих мочевая кислота окисляется под воздействием печеночной урокиназы до растворимого продукта аллонтоина, в виде которого и выводится из организма. Свободные пурины в небольших количествах имеются в моче, кале, а также в тканевых жидкостях.
2. Определение
Подагра – заболевание, обусловленное нарушением пуринового обмена и накоплением мочевой кислоты в организме.
Подагра проявляется одним или несколькими из следующих симптомов: 1) гиперурикемией; 2) приступами острого артрита (обычно моноартрита); 3) образованием подагрических тофусов в околосуставных и других тканях; 4) урикозурией; 5) кристаллизацией солей мочевой кислоты (уратов) в интерстициальной ткани почек и 6) мочекаменной болезнью.
Гиперурикемия – концентрация мочевой кислоты в сыворотке (или плазме) больше 416 мкмоль/л (7 мг%) – основной симптом заболевания и предпосылка развития других проявлений подагры. Гиперурикемия свидетельствует о повышении общего количества мочевой кислоты в организме.
Причиной гиперурикемии могут быть: 1. повышенное образование мочевой кислоты (метаболическая гиперурикемия), 2. нарушение ее выделения (почечная гиперурикемия) или сочетание этих двух механизмов.
Гиперурикемия и гиперурикозурия встречаются в общей популяции не намного реже, чем сахарный диабет 2-го типа и ожирение. Среди органов-мишеней в первую очередь следует назвать синовиальную оболочку суставов и почки.
Суставную подагру считают основным проявлением гиперурикемии. Клиническая картина подагры развивается, когда плазма и внеклеточная жидкость пересыщаются мочевой кислотой и уратные кристаллы начинают откладываться в тканях.
Подагра обычно рассматривается как болезнь суставов обменного характера с частым поражением почек. В Международной классификации болезней она отнесена к кристаллическим артритам. Суставной синдром – наиболее яркое проявление подагры, однако он скорее находится на вершине горы, чем у ее основания. Те или иные висцеральные признаки подагры обнаруживаются еще до развития типичного подагрического артрита (иногда задолго).
По данным медицинской статистики почечные колики или бессимптомный нефролитиаз имелись у 35% больных, артериальная гипертензия – у 62%, мочевой синдром у 25% еще при отсутствии суставного синдрома.
Подагра может длительно протекать без типичных болей в суставах или с 1-2 приступами и последующим многолетним благополучным периодом, поражая внутренние органы, прежде всего почки. Таким образом, диагностика на стадии артрита уже является поздней.
3. Историческая справка
Первый подагрик, имя которого сохранила история, тиран Сиракуз Гиерон жил в V в. до н.э. Далее подагра, это болезнь «столиц» (morbus dominorum), облюбовывала поочередно все возвышающиеся города древности (Афины, Александрию, Рим, Константинополь). Позднее классической страною подагры стала Англия, а затем Голландия.
Д.Г.Рохлин в книге «Болезни древних людей» описывает обнаруженные им при раскопках богатых погребений в Новгороде плюсневые кости со следами подагры («…вот следствие постоянных пиров с объеданием, возлияниями»).
Подагру умоляли о пощаде: «Будь милостива к нам, ты, всему миру известная и всех устрашающая подагра, пусть причиняемая тобою боль будет легкой и кратковременной, а не ужасной и невыносимой, пусть она не превращает нас в калек» (Лукиан).
Проходили столетия и в XX в. отмечена новая волна подагрического диатеза: в Западной Европе в послевоенные годы частота болезни возросла в 15-20 раз (бессимптомная гиперурикемия выявляется у 8-14% взрослого населения, яв6ная подагра – у 2% мужчин). В США насчитывается 2 млн. больных.
Возникла тенденция к омоложению болезни, дебют который раньше относился к 35-40 годам. Хотя по прежнему подавляющее большинство больных (95%) составляют мужчины, но неуклонно растет заболеваемость среди женщин (чаще «мужеподобных»).
Сохраняется значение наследственного фактора. В свое время Гаррот (открывший с помощью нитки, опущенной в кровь больного, факт гиперурикемии при подагре) описал семью, в которой подагра неуклонно передавалась по мужской линии в течение 4 веков. Но нередки и спорадические случаи («подагрики-выскочки»).
По-прежнему подагрой чаще заболевают люди с более высоким интеллектом, что связано с кофеиноподобным действием мочевой кислоты.
4. Рапространенность
Среди населения в целом распространенность гиперурикемии составляет 2-13,2%, а подагры – 1,3-3,7%. Чем выше концентрация мочевой кислоты в сыворотке, тем больше вероятность подагры. Согласно одному из исследований, заболеваемость подагрой при концентрации мочевой кислоты в сыворотке более 540 мкмоль/л (9мг%) составила 4,9%, а при концентрации 415-535 мкмоль/л (7-9 мг%) – 0,5%.
5. Причины
Метаболическая гиперурикемия
Первичная идиопатическая гиперурикемия
Недостаточность гипоксантинфосфорибозилтрансферазы
Избыточная активность фосфорибозилпирофосфатсинтетазы
Гемолиз
Лимфопролиферативные заболевания
Миелопролиферативные заболевания
Эритемия (болезнь Вакеза)
Псориаз
Болезнь Педжета
Гликогенозы типов III, V и VII
Рабдомиолиз
Физическая нагрузка
Употребление алкоголя
Ожирение
Высокое содержание пуринов в пище
Почечная гиперурикемия
Первичная идиопатическая гиперурикемия
Почечная недостаточность
Поликистоз почек
Несахарный диабет
Артериальная гипертония
Ацидоз (лактацидоз, диабетический кетоацидоз, кетоацидоз при голодании)
Бериллиоз
Саркоидоз
Свинцовое отравление
Отравление этанолом
Гиперпаратиреоз
Гипотиреоз
Преэклампсия
Синдром Бартера
Синдром Дауна
Прием лекарственных средств (салицилаты(> 2 г/сут, тиазидовые диуретики, реже петлевые, противотуберкулезные средства — этамбутол,рифампицин, НПВП, препараты инсулина, цитостатики, циклоспорин, никотиновая кислота, цианкобаламин и др.)
Шок
Голодание
Смешанная гиперурикемия
Гликогеноз типа I
Непереносимость фруктозы (недостаточность фруктозодифосфатальдолазы)
Употребление алкоголя
Метаболическая гиперурикемия. Концентрация мочевой кислоты в сыворотке зависит от содержания пуринов в рационе. Около 50% пуринов РНК и 25% пуринов ДНК, поступающих с пищей, выводятся с мочой в виде мочевой кислоты, поэтому употребление продуктов с высоким содержанием нуклеиновых кислот (печень, почки, зобная и поджелудочная железы, анчоусы) оказывает значительное влияние на концентрацию мочевой кислоты в сыворотке. Исключение этих продуктов из рациона приводит к снижению концентрации мочевой кислоты в сыворотке на 60 мкмоль/л (1 мг%) и ее экскреции с мочой – примерно на 1,2 ммоль/сут (200 мг/сут).
Образование пуринов из эндогенных источников также влияет на концентрацию мочевой кислоты в сыворотке. Синтез пуринового кольца из предшественников происходит в 11 этапов и завершается образованием инозинмонофосфата. На первом этапе амидофосфорибозилтрансфераза катализирует взаимодействие фосфорибозилпирофосфата с глутамином. Эта реакция в значительной мере определяет скорость синтеза пуринов и образования мочевой кислоты. Активность амидофосфорибозилтрансферазы возрастает в присутствии фосфорибозилпирофосфата, но ингибируется инозинмонофосфатом и другими рибонуклеотидами. Кроме того, существует регулируемый путь регенерации пуриновых нуклеотидов: гипоксантинфосфорибозилтрансфераза катализирует взаимодействие гипоксантина или гуанина с фосфорибозилпирофосфатом и образование соответствующих рибонуклеотидов – инозинмонофосфата и ГМФ. Ускорение регенерации истощает запасы фосфорибозилпирофосфата и увеличивает концентрацию рибонуклеотидов, что приводит к подавлению активности амидофосфорибозилтрансферазы и синтеза пуринов из предшественников.
В энергетическом обмене важную роль играет взаимопревращение инозинмонофосфата и АМФ – так называемый пуриновый цикл.
Описано Х-сцепленное заболевание, при котором избыточная активность фосфорибозилпирофосфатсинтетазы приводит к накоплению фосфорибозилпирофосфата. В результате ускоряется синтез пуриновых оснований, поскольку фосфорибозилпирофосфат является не только субстратом, но и активатором амидофосфорибозилтрансферазы. При этом заболевании наблюдаются гиперурикемия, повышенная экскреция мочевой кислоты с мочой, развитие подагры и мочекаменной болезни в возрасте до 20 лет.
При Х-сцепленной недостаточности гипоксантин-фосфорибозилтрансферазы угнетается путь регенерации пуриновых нуклеотидов. В результате также накапливается фосфорибозилпирофосфат, а кроме того, снижаются концентрации ингибиторов амидофосфорибозилтрансферазы – инозинмонофосфата и ГМФ. Все это ускоряет синтез пуринов и образование мочевой кислоты, что проявляется гиперурикемией, повышением концентрации мочевой кислоты в моче, мочекаменной болезнью и артритом. Полное отсутствие гипоксантинфосфорибозилтрансферазы носит название синдром Леша-Найхана и сопровождается психическими и неврологическими расстройствами – агрессивным поведением со склонностью к самоповреждению, хореоатетозом. Частичная недостаточность фермента (синдром Келли-Зигмиллера) проявляется подагрическим артритом и мочекаменной болезнью.
Причиной гиперурикемии может быть повышение катаболизма пуриновых нуклеотидов при усиленной пролиферации, массовой гибели и распаде клеток, например при бластном кризе, химиотерапии злокачественных новообразований (синдром распада опухоли), гемолизе и рабдомиолизе. Нуклеиновые кислоты, высвобождаемые из погибающих клеток, распадаются под действием нуклеаз и фосфодиэстераз до нуклеозидмонофосфатов, которые последовательно превращаются в нуклеозиды, азотистые основания и мочевую кислоту. Усиленный распад мышечного АТФ при тяжелой физической нагрузке, эпилептическом статусе и гликогенозах типов III, V и VII тоже может привести к гиперурикемии. Возможно, что гиперурикемия при инфаркте миокарда, отравлении продуктами горения и острой дыхательной недостаточности также связана с распадом АТФ.
Почечная гиперурикемия. Экскреция мочевой кислоты нарушена у 98% больных с первичной гипоурикемией и подагрой. Об этом свидетельствует более низкое, чем в норме, отношение клиренса мочевой кислоты к СКФ. В результате при любой концентрации мочевой кислоты в сыворотке ее экскреция при подагре на 40% меньше, чем у здорового человека, и наоборот, одинаковый клиренс достигается только в том случае, если концентрация мочевой кислоты в сыворотке у больного подагрой выше на 60-120 мкмоль/л (1-2 мг%), чем у здорового человека. При поступлении пуринов с пищей или их в/в введении экскреция мочевой кислоты ускоряется как у больных подагрой, так и у здоровых людей.
Экскреция мочевой кислоты может уменьшаться в результате снижения СКФ, уменьшения секреции или повышения реабсорбции. Снижение СКФ способствует развитию вторичной гиперурикемии при почечной недостаточности. Хронические заболевания почек всегда сопровождаются гиперурикемией, но при этом нет прямой зависимости между концентрацией мочевой кислоты в сыворотке, с одной стороны, и концентрацией креатинина – с другой.
При ХПН отношение клиренса мочевой кислоты к СКФ постепенно повышается, канальцевая секреция не меняется, реабсорбция снижается, и по мере усугубления почечной недостаточности все больше мочевой кислоты выводится с калом.
Снижение секреции мочевой кислоты в проксимальных канальцах может привести к гиперурикемии и при нормальной скорости образования мочевой кислоты. Этим объясняется вторичная гиперурикемия при ацидозе. Диабетический кетоацидоз, голодание, лактацидоз, отравление этанолом или салицилатами приводят к накоплению органических кислот (β-оксимасляной, ацетоуксусной, молочной, салициловой), которые конкурируют с мочевой кислотой за транспортные системы, обеспечивающие секрецию. Усиление реабсорбции в дистальных отделах проксимальных канальцев также может привезти к гиперурикемии и подагре. Это наблюдается при снижении объема внеклеточной жидкости, например при несахарном диабете или приеме диуретиков.
Смешанная гиперурикемия. Иногда причиной гиперурикемии бывает сочетание повышенного образования мочевой кислоты и сниженного ее выведения. При гликогенозе типа I (недостаточности глюкозо-6-фосфатазы, катализирующей превращение глюкозо-6-фосфата в глюкозу) уже в грудном возрасте появляется гиперурикемия и рано развивается подагра. Повышение продукции мочевой кислоты в этом случае связано с распадом АТФ во время голодания или гипогликемии. Кроме того, у таких больных снижена концентрация нуклеозидмонофосфатов, что приводит к уменьшению их ингибирующего действия на амидофосфорибозилтрансферазу и усилению образования пуринов. Наконец, у них часто возрастает концентрация молочной кислоты в крови, а это сопровождается угнетением канальцевой секреции мочевой кислоты.
Оба механизма развития гиперурикемии действуют и при непереносимости фруктозы, связанной с недостаточностью фруктозодифосфатальдолазы. У таких больных прием фруктозы приводит к накоплению фруктозо-1-фосфата, истощению запасов АТФ, усилению катаболизма пуриновых нуклеотидов и гиперурикемии. Лактацидоз и почечный канальцевый ацидоз приводят к задержке мочевой кислоты в организме. У гомозигот после приема фруктозы наблюдаются рвота, гипогликемия, а продолжительное потребление фруктозы приводит к печеночной недостаточности и нарушению функции почечных канальцев. У гетерозигот развивается гиперурикемия, а примерно у трети из них – подагра. По-видимому, это довольно частая причина семейной подагры, так как распространенность гетерозигот составляет 1:80 – 1:250.
Злоупотребление алкоголем также вызывает смешанную гиперурикемию путем: 1) стимуляции распада АТФ и усиления образования мочевой кислоты в печени и 2) нарушения секреции мочевой кислоты в почках за счет ацидоза. Кроме того, в некоторых спиртных напитках, например в пиве, содержится много пуринов.
6. Клинические проявления
Подагра может проявляться по-разному, но для типичного развития болезни характерны три стадии: бессимптомная, гиперурикемическая, интермитирующая подагра с периодически возникающими приступами острого артрита и хроническая подагра, для которой характерно появление тофусов. Поражения почек, в том числе мочекаменная болезнь могут развиваться как до, так и после первого приступа подагрического артрита.
Течение подагры зависит от продолжительности и тяжести гиперурикемии. Первый приступ подагры чаще всего возникает через 20-40 лет стойкой гиперурикемии: у мужчин это обычно происходит в возрасте 40-60 лет, а у женщин – после наступления менопаузы.
Подагрический артрит. Самое яркое проявление подагры – острый моноартрит. Первый приступ начинается внезапно и сопровождается сильной болью и признаками воспаления: кожа над суставом красная, горячая, отечная, пальпация сустава резко болезненна; иногда наблюдается лихорадка. У некоторых больных приступу предшествуют продромальный период или продолжающиеся несколько часов приступы менее интенсивной боли. При отсутствии лечения симптомы нарастают в течение 24-48ч, а затем начинают ослабевать и проходят через 7-10 суток. После приступа над пораженным суставом возможно шелушение кожи.
При первом приступе обычно поражается один сустав, реже (в основном у женщин) – несколько суставов. Чаще всего это суставы ног. Реже наблюдаются внесуставная локализация воспаления, например подошвенный фасциит, ахилобурсит, воспаление узелков Гебердена. У 90% больных поражается первый плюснефаланговый сустав, причем у 50% — во время первого приступа подагры. Сакроилеит, спондилоартрит и поражение синхондроза рукоятки грудины встречаются редко.
Причиной приступа может послужить любой фактор, вызывающий резкие колебания концентрации мочевой кислоты в сыворотке, в основном – ее уменьшение. Теоретически внезапное увеличение концентрации мочевой кислоты может привести к образованию новых кристаллов, в то время как снижение концентрации мочевой кислоты в сыворотке и межклеточной жидкости – к частичному растворению и фрагментации раннее образованных кристаллов. Предрасполагающие факторы – стресс, травмы, инфекции, хирургические вмешательства, пребывание в больнице, голодание, похудание, переедание, употребление спиртных напитков и прием лекарственных средств. Наибольшее значение имеют пребывание в больнице и прием лекарственных средств. У 20-86% больных подагрой при госпитализации развивается острый артрит. Причинами его могут быть тяжелые сопутствующие болезни, назначение новых лекарственных средств, водно-электролитные нарушения и общая анестезия. Приступ подагры может развиваться при лечении тиазидными диуретиками, и в начале лечения аллопуринолом и другими гипоурикемическими средствами.
При травмах и отеках объем синовиальной жидкости с нормальной концентрацией мочевой кислоты увеличивается. В ходе лечения вода покидает суставную полость намного быстрее, чем мочевая кислота, поэтому ее концентрация в синовиальной жидкости временно возрастает, создавая условия для кристаллизации и развития острого артирита. В этих случаях гиперурикемию так и не удается подтвердить, несмотря на многократные попытки.
В межприступном периоде боль в суставах отсутствует. В тяжелых случаях, особенно в отсутствие лечения, со временем развивается хронический подагрический артрит. Промежутки между приступами укорачиваются, а сами приступы становятся более продолжительными и поражают уже не один, а несколько суставов. Хотя боль может быть и не столь сильной. Хроническая подагра представляет собой полиартрит с постоянной неинтенсивной болью и острым и подострым воспалением. При физикальном исследовании обнаруживают тофусы. Скорость кристаллизации уратов, а также деструкции суставов зависит от тяжести и продолжительности гиперурикемии. Обычно между первым приступом подагры и проявлением тофусов проходит около 10 лет. В это время происходит постепенная деструкция хрящевой и костной тканей, признаки которой можно обнаружить при рентгенологическом исследовании.
Патогенез. Острый приступ подагры вызывает реакция нейтрофилов на уратные кристаллы, приводящая к активации гуморальных и клеточных механизмов воспаления. Уратные кристаллы активируют комплемент как по классическому, так и по альтернативному пути. Кроме того, происходит активация фактора свертывания XII (фактор Хагемана), стимулирующего образование брадикинина , калликреина и плазмина. Под действием уратных кристаллов из нейтрофилов высвобождаются лизосомные ферменты, свободные радикалы кислорода, метаболиты лейкотриенов и простагландинов, коллагеназа и другие протеазы. Фагоцитоз кристаллов нейтрофилами приводит к выбросу лейкотриена В4. Лейкотриен В4 и фрагмент комплемента С5а вызывают хемотаксис нейтрофилов в начальной фазе острого приступа подагры. Со временем на смену нейтрофилам приходят макрофаги. Под действием уратных кристаллов из макрофагов высвобождаются простагландины (простагландин Е2), лизосомные ферменты, ФНОα, ИЛ-1 и ИЛ-6. Синовиоциты тоже участвуют в развитии воспаления, выделяя ИЛ-8 и другие цитокины.
Некоторые белки плазмы влияют на способность уратных кристаллов вызывать воспаление. Так, абсорбированный очищенный IgG усиливает высвобождение вазоактивных веществ из тромбоцитов под действием кристаллов, образование супероксидного радикала и выброс лизосомных ферментов из нейтрофилов. С другой стороны, апопротеин В, входящий в состав ЛПОНП, ЛПНП и ЛППП, ослабляет активирующее действие уратных кристаллов на нейтрофилы. В норме апопротеин В отсутствует в синовиальной жидкости, поскольку липопротеиды не проникают через гематосиновиальный барьер. При воспалении проницаемость синовиальной оболочки повышается, проникают в полость сустава, связываются с уратными кристаллами и, возможно, способствуют прекращению приступа.
Классический острый приступ подагры
- Провоцирующие моменты – длительная ходьба, травма, охлаждение, употребление алкоголя и пищи, богатой пуринами, умственное перенапряжение (наиболее тяжелые приступы наблюдались у Сиденгама, когда он заканчивал в 1683 г свой «Тракт о подагре и водянке»).
- Предвестники приступа – большинство больных за несколько дней могут предсказать приступ. Возникают головные боли, раздражительность, мрачные мысли, припадки гнева, снижение работоспособности. Но иногда, напротив, ощущается эйфория, подъем сил («яркое солнце перед бурей» — по Сиденгаму).
- Время наступления приступа – чаще ночью, у многих – ближе к утру («с криком первых петухов»)
- Поражаемые суставы – в половине случаев или еще чаще – I плюснефаланговый сустав. Реже – голеностопный, коленный. Очень редко – суставы рук
- Жалобы – резчайшие боли в суставе в покое, движения невозможны, больные не могут терпеть даже прикосновения одеяла.
- Объективные данные – опухание сустав, местная гипертермия, кожа над суставом темно-красная («цвета пиона»), напряженная, блестящая. Отмечается набухание местных вен, вены выступают над кожей, варикозные. Повышение температуры тела до 38-39ºС. Нередко это состояние ошибочно принимают за гнойный артрит, рожистое воспаление
- Реакция больного на приступ – крайняя раздражительность, душевные страдания.
- Патогенез приступа – кристаллизация аратов, фагоцитоз кристаллов лейкоцитами, высвобождение большого количества лизосомальных ферментов, участие также кининов и простагландинов.
Приступ продолжается обычно несколько дней. Затем все симптомы исчезают (могут оставаться шелушение, и зуд кожи над суставом), функция сустава полностью восстанавливается. Обычно применяют критерии артрита АРА (1977):
- В анамнезе у больных имеется более чем одна острая атака артрита.
- Воспаление сустава достигает максимума уже в первые сутки.
- Моноартикулярный характер артрита.
- Гиперемия кожи над пораженным суставом.
- Припухание или боль, локализованные в 1-м плюснефаланговом суставе.
- Одностороннее поражение суставов свода стопы.
- Узелковые образования, напоминающие тофусы.
- Гиперурикемия.
- Одностороннее поражение 1-го плюснефалангового сустава.
- Асимметрическое припухание пораженного сустава.
- На рентгенограммах обнаруживаются субкортикальные кисты без эрозий.
- отсутствует флора в суставной жидкости.
Типичная особенность подагричесого артрита — полная обратимость признаков островоспалительного поражения сустава (деформация, гиперемия, боль) при купировании приступа.
Однако, в последующем (без лечения) приступы учащаются, удлиняются, происходит вовлечение новых суставов. Постепенно, за 5-6 лет и больного, формируется хроническая подагрическая артропатия.
Признаки хронической артропатии
Клинические
Постепенно развивается деформация пораженных суставов за счет отложения уратов и присоединения вторичного остеоартроза. «Разнообразие, которое при этом наблюдается, не поддается описанию» (Флоран). В тяжелых случаях «конечность становится похожей на пучок корней пастернака» (Сиденгам). Нарушается функция суставов. «Подагрик тащится, точно хромой, с таким трудом, что кажется, будто он останется на месте» (Сиденгам).
Лабораторные
- В период обострения – воспалительные сдвиги биохимических показателей (СРБ, сиаловые кислоты, альфа2-глобулины и др.).
- Отрицательная реакция на ревматойдный фактор.
- Синовиальная жидкость имеет низкую вязкость, высокий цитоз с преобладанием полисегментированных нейтрофилов. Патогноманично – обнаружение игольчатых двоякопреломляющих кристаллов урата натрия.
Рентгенологические
- Симптом «пробойников» — скопления уратов в костях в виде округлых просветлений (костные тофусы), например, в головке I плюсневой кости.
- Остеопороз.
- Вторичный остеоартроз (сужение суставных щелей, остеофиты, анкилозы — «бугристая подагрическая стопа»).
Наслоение вторичного артроза затрудняет дифференциальную диагностику между подагрой и первичным деформирующим остеоартрозом.
Уратная нефропатия
У тебя камни в почках, а у меня подагра: мы поженились на родных сестрах.
Из письма Эразма Роттердамского Томасу Мору
На связь между подагрой и мочекаменной болезнью (МКБ) указывал еще Парацельс. Позднее выяснились как большая частота (60-70% случаев), так и многообразие почечных поражений при подагре. Обобщающим для них служит термин «уратная нефропатия», включающая несколько вариантов.
1. Уратный нефролитиаз
МКБ наблюдается у 20-40% больных подагрой. Симптоматика МКБ может появиться на фоне суставных приступов, но иногда и предшествует им. Типичны почечные колики, кислая реакция мочи (рН<5,4), обилие уратов в осадке мочи. При УЗИ почек выявляются камни и типичные для подагры кистозные изменения в паренхиме. Часто развивается АГ, ожирение, рецидивирующие почечные колики.
2. Вторичный пиелонефрит
Проявляется обычными симптомами: повышение температуры, дизурия, лейкоцитурия и бактериурия. Выявляется деформация чашечно-лоханочной системы по данным УЗИ и внутривенной урографии.
3. Хронический уратный тубулоинтерстициальный нефрит (ХТИН)
Повышение фильтрации и секреции уратов в моче при подагре приводит к их отложению в мозговом, реже корковом слое. Отложения носят очаговый характер (микротофусы в интерстиции). Клинически процесс проявляется незначительной («следовой» канальцевой – преимущественно b2-микроглобулин) протеинурией, которой может и не быть, лейкоцитурией и микрогематурией, небольшим количеством уратов в моче.
 |
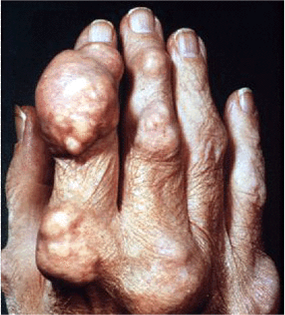 |
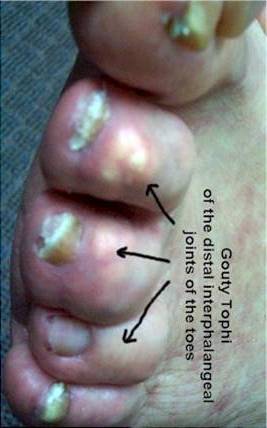
| Рисунок 1. Подагрический артрит суставов пальцев стопы | Рисунок 2. Подагрический артрит суставов кисти, тофусы |
 |
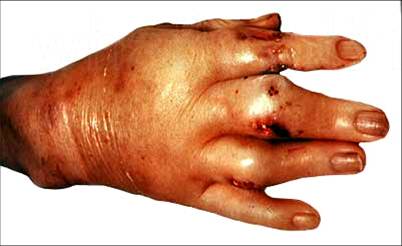 |
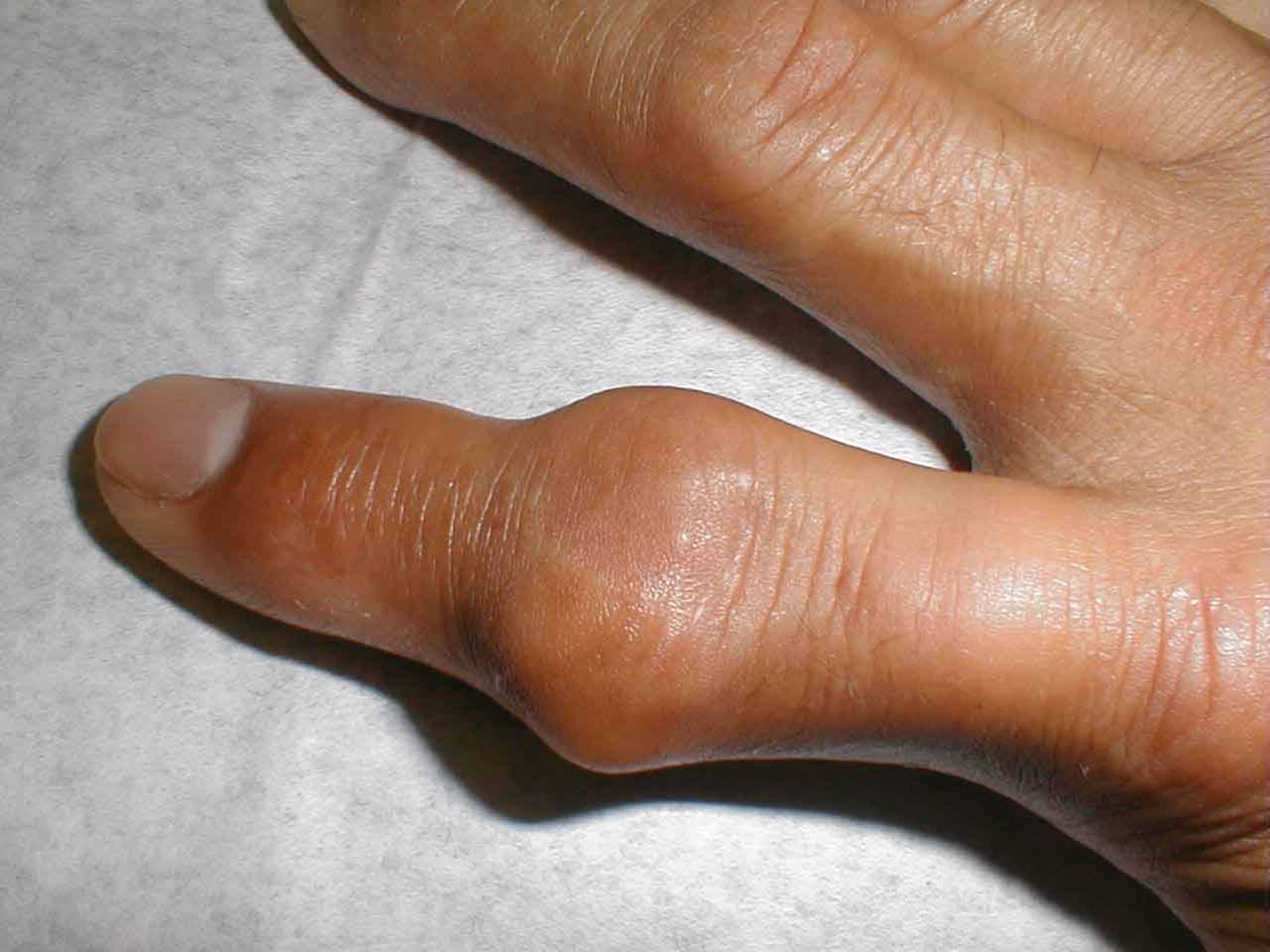
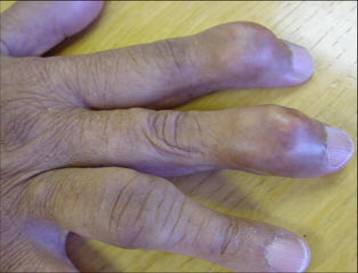
| Рисунок 3. Подагрический артрит межфалангового сустава кисти | Рисунок 4. Кисть правой руки при подагре, тофусы |
 |
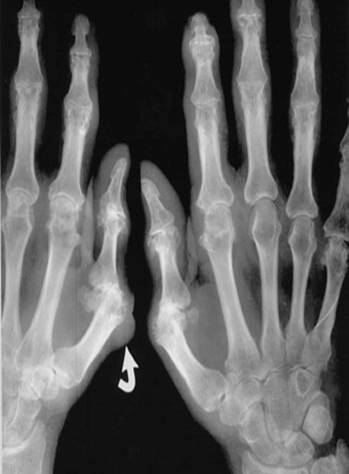 |
| Рисунок 5. Подагрический артрит суставов кисти | Рисунок 6. Рентгенограмма кистей при подагрическом артрите |
Специальный тест – обнаружение в моче снижения активности канальцевого фермента N-ацетил-b-D-глюкозаминидазы (НАГ). Уменьшение активности НАГ является ранним признаком хронического уратного тубулоинтерстициального нефрита, хотя может быть признаком любого другого ХТИН.
Почти у 1/3 больных развивается артериальная гипертензия, чаще с кризовым характером течения. Нарушается концентрационная способность почек (снижение относительной плотности мочи), подавление фибринолиза (снижение концентрации урокиназы) и дисфункция эндотелия (эндотелин-1) локально в почке под действием мочевой кислоты приводят к прогрессирующему фиброзу тубуло-интерстициальной ткани почек, и постепенному прогрессированию ХПН, от которой погибают 15-20% больных подагрой. ХТИН – одно из самых частых проявлений уратных нефропатий, способных приводить к терминальной почечной недостаточности. Формирование ХТИН может происходить уже на стадии гиперурикозурии, предшествуя первой атаке суставной подагры, причем у части больных подагрический артрит не наблюдается вообще. ХТИН долго остается нераспознанным в связи с малой специфичностью симптомов. В дальнейшем урикозурия снижается, что свидетельствует о выраженном нарушении функции почек, и начинает нарастать гиперурикемия, на фоне чего АГ становится высокой и стойкой.
4. Острая мочекислая нефропатия (блокада почечных канальцев)
В основе – массивная имбибиция мочекислым натрием почечных канальцев. Возникают резкие боли в пояснице с обеих сторон, моча становится бурой, олигурия сменяться анурией, развитием прогрессирующей ОПН (нарастание концентрации креатинина и калия, АГ, острая левожелудочковая недостаточность с развитием отека легких, возможно фатального).
Провоцировать приступ могут чрезмерная физическая нагрузка, перегревание, ограничение жидкости, прием алкоголя, употребление большого количества мясной пищи, передозировка диуретиков, в гематологической и онкологической практике при лучевой и химиотерапии в результате массивного распада тканей.
5. Иммунокомплексный гломерулонефрит с гиперурикемией.
Форма, описанная недавно, патогенез которой нуждается в уточнении. Остается не вполне ясным, является ли мочевая кислота прямым индуктором иммунного воспаления клубочков или имеется сочетание особой клинической формы хронического гломерулонефрита с гиперурикемией. Заболевание протекает как хронический латентный гломерулонефрит с микрогематурией, умеренной протеинурией. Иногда возникают эпизоды макрогематурии. Нефротический синдром, как правило, не развивается. Часто развивается АГ. Возможно раннее нарушение концентрационной функции почек. Морфологически – картина мезангиопролиферативного нефрита с отложениями IgG и комплемента, выражен тубулоинтерстициальный компонент.
Нередко поражения почек при гиперурикемии могут быть комбинированными, а также могут сочетаться с другими хроническими нефропатиями — аналгетической, диабетической и ишемическим поражением почек, особенно у пожилых больных.
Подагрические тофусы
Тофусы-– это скопления кристаллов моногидрата мононатриевой соли мочевой кислоты, окруженные гигантскими клетками, имеющие вид узелков, картина напоминает гранулему инородного тела. Они образуются как в суставах, так и в околосуставных тканях. Разрушая костную, хрящевую и мягкие ткани, они вызывают деформацию и вторичные дегенеративные изменения суставов(впервые были описаны Галеном). Они являются важным диагностическим признаком подагры («подагрические печати»), свидетельствуют о большой давности заболевания (более 4-5 лет) и, как правило, об очень высокой урикемии.
Типичная локализация тофусов – хрящи ушных раковин (при этом они никогда не располагаются в мочке уха), тыльная поверхность пальцев (узелки Гебердена всегда располагаются на боковых поверхностях!), область ахилловых сухожилий, локтевых суставов, иногда – у крыльев носа. Размер их колеблется от булавочной головки до ореха или некрупного яйца, цвет – желтовато белый. Возможно вскрытие узлов с выделением через свищи беловатой массы, которую раньше сравнивали со сметаной или мелом, растворенным в воде, а в наше время – с зубной пастой. Тофусы редко инфицируются (бактерицидное действие уратов), хирургические вмешательства в области тофусов нежелательны из-за плохого заживления ран.
Подагра и ассоциированные заболевания
Подагра часто сочетается с другими «обменными» заболеваниями: ожирение, сахарный диабет, желчнокаменная болезнь, атеросклероз.
«Подагра для артерий то же, что ревматизм для сердца», — полагал Юмар (это, несомненно, преувеличение).
Тем не менее, в наше время гиперурикемия считается одним из факторов риска ИБС.
Все большее количество исследований подтверждает значение гиперурикемии как кардиоваскулярного фактора риска. Наличие гиперурикемии повышает риск сердечно-сосудистых заболеваний, в т.ч. ишемической болезни сердца, в 1,37 раза (исследование Honolulu Heat Program), риск смерти от ИБС в 1,62 раза (Chicago Heat Association). По данным исследования PIUMA при повышении концентрации сывороточного креатинина риск вероятности сердечно-сосудистых осложнений увеличивается в 1,73 раза, в том числе фатальных – в 1,96 раза. Атеросклероз у больных подагрой встречается в 10 раз чаще, чем в общей популяции.
У 68% больных подагрой выявляется метаболический синдром, что связано с проявлениями атеросклероза и сахарного диабета. Терапия сахарного диабета с помощью метформина (сиофора) достоверно снижает уровень глюкозы, холестерина, липопротеинов высокой и низкой плотности и почти у половины больных достигается нормоурикемия.
Артериальная гипертензия при уратном дисметаболизме, как правило, высокая и хуже поддается антигипертензивной терапии.
7. Критерии подагры
Всемирная организация здравоохранения.
А. Выявление кристаллов уратов в синовиальной жидкости
В. Верификация кристаллов при подозрении на тофусы
С. Анализ 12 клинико-лабораторных признаков (для диагноза необходимо не менее 6):
1. Максимальное воспаление сустава в первый день
2. Наличие более чем одной атаки артрита
3. Моноартрит
4. Покраснение сустава
5. Боль и воспаление проксимального фалангового сустава І пальца
6. Ассиметричное воспаление плюсне-фаланговых суставов
7. Одностороннее поражение дорзальных суставов
8. Подозрение на тофусы
9. Гипреурикемия
10. Ассиметричное воспаление суставов
11. Субкортикальные кисты без эрозии при рентгенологическом исследовании
12. Отсутствие микроорганизмов в культуре синовиальной жидкости
8. Оценка пуринового обмена при подагре
Для достоверности оценки нарушений пуринового обмена при подагре в идеале следует определить:
- Уровень мочевой кислоты в сыворотке крови. В это время не рекомендуется принимать таких препаратов, как кофеин, теобромин, салицилаты, антидиабетические сульфаниламиды. Следует учитывать, что максимальный уровень мочевой кислоты отмечается около 11 часов утра. Сыворотку надо исследовать не позднее 6 часов с момента взятия крови. В норме уровень мочевой кислоты в сыворотке на обычной диете равен 0,26-0,40ммоль/л, на малопуриновой диете – 0,21-0,32 ммоль/л. Критерием подагры считается уровень более 0,36 ммоль/л для женщин и более 0,42 ммоль/л для мужчин
- Выделение мочевой кислоты с мочой за сутки. Норма – 1,8 – 3,6 ммоль (300-6000 мг) в сутки.
- Почечный клиренс мочевой кислоты. Норма – 6-7 мл/мин.
- Оценка синовиальной жидкости на наличие мочевой кислоты и ее кристаллов.
Для выбора адекватного лечения желательно установить тип подагры.
Таблица 1. Основные типы подагры.
| Признак | Метаболический тип (гиперпродукционная подагра) | Почечный тип (гипоэкскреторная) |
| Основной патогенетический механизм | Повышенная продукция мочевой кислоты в организме | Недостаточное выведение мочевой кислоты с мочой |
| Частота | Встречается часто | Редко |
| Уровень мочевой кислоты в крови | Наиболее высокий (может доходить до 0,8-0,9 ммоль/л) | Умеренное повышение |
| Выделение мочевой кислоты с мочой | Высокая урикозурия (более 3,6 ммоль в сутки, может быть и более 6,0 ммоль) | Ниже нормы (менее 1,8 ммоль в сутки) |
| Клиренс мочевой кислоты | Нормальный | Снижен (3,0 – 3,5 мл/мин) |
| Риск преципитации уратов в собирательных трубочках | Высокий | Меньше |
| Особенности лечения | Противопоказаны урикозурические средства | Эти средства могут быть применены |
Примечание. Выделяется также смешанный тип подагры, при котором сочетаются оба патогенетических механизма и который клинически протекает наиболее тяжело.
Вторичная подагра
Во избежание диагностических ошибок необходимо помнить о вторичных нарушениях метаболизма уратов при следующих состояниях:
- Уремическая псевдоподагра – нарушение выделения и накопления мочевой кислоты при ХПН в финале какого-либо другого заболевания почек (хронический гломерулонефрит, поликистоз и др.).
- Лечение цитостатиками гематологических заболеваний (хронический миелолейкоз, полицитемия, миеломная болезнь и др.): «освобождение пуринов» при массивной гибели клеток. Профилактика этого осложнения включает прием аллопуринола в дозе 600-900 мг в сутки за 5 дней до химиотерапии, а также обильное питье и ощелачивание мочи.
- Лучевая и цитостатическая терапия больных злокачественными новообразованиями («синдром распада опухоли»).
- Свинцовая интоксикация («вторичная подагра сатирников»).
- Вторичная лекарственная подагра при длительном лечении диуретиками (фуросемид, гипотиазид), экстрактами печени, салицилатами.
9. Классификация
Коды МКБ-10: М 10.0–10.9
Таблица 2. Классификация подагры.
| Этиологическая характеристика | Форма поражения суставов | Периферические тофусы | Тип нефропатии |
| 1. Первичная подагра
2. Вторичная подагра |
1. Острый артрит
2.Интермитирующий артрит: а) обострение б) ремиссия 3. Хронический артрит: а) обострение б) ремиссия 4. Безартритный вариант болезни |
1. Имеются
2. Отсутствуют |
Острая мочекислая нефропатия
ХТИН Уролитиаз Хронический пиелонефрит Хронический гломерулонефрит |
Примеры клинического диагноза:
Первичная подагра. Острый артрит плюснефалангового сустава первого пальца стопы слева, хронический артрит коленных суставов, обострение, уратная нефропатия: хронический тубуло-интерстициальный нефрит, МКБ, камни обеих почек, ХБП 2 ст.
10. Лечение
У врачеванья нет средств с узловатой подагрою сладить.
Овидий
Радикальное и усовершенствованное лечение,
способное освободить от подагрического диатеза,
покоится еще в колодце Демокрита.
Сиденгам
Все лечение подагры – это терпение и фланель.
Куллэн
Эти пессимистические высказывания приводятся только для того, чтобы подчеркнуть несомненные успехи в лечении подагры в наше время.
Купирование приступа подагры
Общие меры
- Полный покой. Возвышенное положение конечности. Под больную ногу положить подушку. Давление одеяла можно избегнуть с помощью специального обруча.
- Местно – холод
- Смазывать сустав каким-либо жиром; обернуть конечность нетолстым (во избежание перегрева) слоем ваты.
- Обильное питье (2,0-2,5 литра жидкости в день) – щелочные растворы, разведенный лимонный сок, молоко, кефир, кисели, компоты. Не употреблять ни мяса, ни рыбы. Рекомендуются овощные супы, жидкие каши.
Медикаментозные средства для купирования приступа
I.Колхицин
- Препарат получается из безвременника осеннего (Colchicum autumnale), который использовался для лечения подагры Яковом Психрестом и Александром из Тралеса в V – VI вв.н.э. и который был известен Авиценне. «Второе рождение» препарата относится к началу XIX в.
- Механизм действия: угнетение миграции лейкоцитов, затруднение фагоцитоза кристаллов уратов, задержка дегрануляции лизосом. Препарат эффективен у 90 % больных.
- Выпуск – таблетки по 0,0006, лечение приступа следует начинать как можно раньше (оптимально – в продромальном периоде). 1-я доза – 0,6 мг, затем – прием по 1 таблетке каждый час до исчезновения симптомов или появления побочных эффектов со стороны ЖКТ (тошнота, рвота и т.д.), но не более 6 мг в первые сутки. В/в введение колхицина (1-2 мг на 20 мл физиологического раствора 2-3 раза в сутки) позволяет избежать влияния на ЖКТ, но оно опасно из-за побочного действия на кроветворение, функцию почек (снижают СКФ до 10 мл/мин), и печени (повышение трансаминаз).
- Улучшение обычно возникает в первые 12 часов. В последующие дни (при улучшении) чаще дают по 2 мг сутки.
- Побочные действия (которым могут препятствовать применению полной дозы в 1-ый день) – это диарея, а также – тошнота, рвота, боли в животе. Развитие диареи иногда предотвращаются приемом препарата колхимакс (где к колхицину добавлены фенобарбитал и опий).Положительный эффект от применения колхицина сам по себе является диагностическим критерием подагры.
II. Нестероидные противовоспалительные средства.
НПВС не столь специфичны как колхицин, но по своим терапевтическим эффектам с ним полностью сопоставимы, особенно в начале приступа. Обычно назначают максимальные дозы и прекращают прием через 3 – 4 дня.
- Диклофенак – 25-50 мг 4 раза в день.
- Напроксен — 1-я доза – 750 мг, далее – по 250 мг каждые 8 часов (или др.)
При назначении НПВП следует учитывать возможность побочных эффектов и осложнений (язвы желудка и ДПК, АГ, нарушение функции почек, нарастание ХСН, гиперкалиемия).
В последние годы привлекли внимание селективные НПВП. Однако было опубликовано лишь одно исследование, в котором сравнивали эффективность селективного ингибитора ЦОГ-2 эторикоксиба с индометацином при подагрическом артрите. Эторикоксиб в дозе 120 мг в день оказывал быстрое благоприятное влияние на острый подагрический артрит, сравнимое с индометацином.
В Институте ревматологии проведено открытое контролируемое исследование (56 больных, возраст от 35 до 79 лет) по эффективности и безопасности нимесулида (препарат «Нимесил», содержащий нимесулид в виде быстрорастворимых гранул) при остром и хроническом подагрическом артрите.
Учитывая мнение экспертов, больным рекомендовался прием препарата до полного купирования артрита и далее несколько дней. Для профилактики быстро наступающего последующего обострения у больных с затяжными рецидивами или хроническим течением артрита рекомендован недельный прием препарата. При сохранении воспалительных явлений лечение продлевается еще на 1 неделю.
При оценке безопасности применения нимесулида у больных подагрическим артритом определялось его влияние на артериальное давление (АД). При применении ручного метода измерения АД не отмечено какого-либо существенного изменения в динамике АД. Применение суточного мониторирования АД (СМАД) показало, что у больных без АГ, получающих нимесулид в гранулированной форме, изменение средних значений систолического АД (САД)/диастолического АД (ДАД) было недостоверным и составило 2-5 мм рт.ст., незначительно менялись показатели вариабельности (ИВ). При 2-недельном приеме препарата показатели СМАД не изменились, а по некоторым значениям даже снизились. Достоверно уменьшилось САД (на 16 мм рт.ст), ДАД (на 8 мм рт.ст), нормализовался суточный ритм. Возможно, что это частично связано со значительным уменьшением болевого синдрома. У трети больных отмечено повышенное АД, максимально до 200/130 мм рт.ст., все эти пациенты получали антигипертензивную терапию (ингибиторы АПФ и β-блокаторы).
III. Кортикостероиды.
- Применять их перорально при остром приступе подагры большинство ревматологов не советуют.
- В тяжелых случаях возможно внутрисуставное введение преднизолона (100 мг в крупный, 50 мг в средний и 25 мг в мелкий сустав), беклометазона (1 мл (7.5 мг) в крупный, 0.5 мл в средний и 0.1–0.25 мл в мелкий сустав).
У пожилых больных в связи с наличием выраженной полиморбидности и больных с рефрактерным подагрическим артритом применение ГКС является практически единственным методом купирования артрита. Определению «рефрактерный подагрический артрит» соответствует полиартикулярное поражение, затяжное течение артрита (более месяца), при этом часто выявляется недостаточная эффективность НПВП. Возможно, что рост распространенности подагры практически совпадает с НПВП-факторами риска (в т.ч. нарушение пуринового обмена), и это свидетельствует о грядущем более широком использовании ГК как важной противовоспалительной линии в лечении подагры.
По наблюдению В.Г.Барсковой (2006), внутривенное введение ГК в течение 2-3 дней в средних дозах 250-500 мг является безопасным методом. Для предупреждения или своевременной коррекции побочных эффектов ГК рекомендуется усилить контролировать АД у больных артериальной гипертензией в эти дни.
Больной подагрой должен постоянно носить с собой препарат, помогающий ему (подобно тому, как больной ИБС должен всегда иметь при себе нитроглицерин), ибо приступ может развиться неожиданно.
Полезно заранее, не дожидаясь приступа, проверить переносимость того или другого препарата (например, колхицина или диклофенака) – в какой-нибудь выходной день в межприступном периоде.
Плановое лечение
Общие рекомендации:
- Избегать физических и эмоциональных перегрузок.
- Снижение по возможности массы тела ь при избыточном весе.
- Активный образ жизни (борьба с гиподинамией).
- При артериальной гипертензии и отеках не употреблять длительно тиазидовые диуретики.
- Воздерживаться от аспирина (в небольших дозах он повышает уровень мочевой кислоты и может спровоцировать криз).
- Употреблять больше жидкостей (если к этому нет противопоказаний).
- Отказ от алкоголя (избыток молочной кислоты поле приема алкоголя тормозит почечную экскрецию уратов). В первую очередь это относится к винам (в особенности портвейну и хересу) и к пиву темных сортов.
Диета
Подагра – это болезнь тех, кто много потребляет
и мало расходует.(Шоффар)
Таблица 3. Диета при подагре.
| Не рекомендуются продукты, богатые пуринами, щавелевой кислотой | Рекомендуется |
| 1. Жареное, жирное мясо, в особенности молодых животных (цыплята и др.). Крепкие мясные и рыбные бульоны (при варке 50-60% пуринов переходит в бульон). Печень, почки, мозги. Тугоплавкие жиры, сало.
2. Сардины, шпроты 3. Бобовые 4. Грибы, салат, щавель, шпинат, цветная капуста, ревень, баклажаны, брюква, редис, соя. 5. Шоколад, чай, кофе, какао 6. Курсы лечебного голодания. |
1. Вареное мясо (взрослых животных), рыба – не чаще 2-3 раз в неделю. Уровень белков в диете не должен превышать 1 г/кг массы. Куриное мясо – содержит относительно меньше пуринов.
2. Яйца 3. Молоко и молочные продукты, сыр 4. Овощи (кроме соленых и маринованных). 5. Фрукты (особенно цитрусовые из-за их ощелачивающего эффекта). 6. Ягоды (кроме малины). 7. Крупы, картофель. 8. Щелочные минеральные воды 9. Разгрузочные дни (1 раз в неделю) – овощные, фруктовые, творожно-кефирные, молочные. |
Общие принципы лечений препаратами, нормализующими пуриновый обмен:
- Нельзя начинать лечение в период острого приступа (только в межприступный период), так как их применение может увеличивать концентрацию пуринов в сыворотке в начале лечения, при этом основные проявления острой подагры могут нарастать (суставной синдром, почечный).
- Длительный (годами) прием препаратов. Возможны небольшие паузы (по 2-4 недели) в период нормализации уровня мочевой кислоты в крови.
- Учитывать тип нарушений пуринового обмена (метаболический, почечный, смешанный). Если тип не установлен, применять урикоингибиторы, но не использовать урикозурические средства.
- Поддерживать суточный диурез около 2 литров (потребление около 2,5 литров жидкости в сутки), использовать подщелачивание мочи.
- Поскольку в первые дни лечения повышается опасность суставных кризов, осуществлять в это время профилактику колхицином (1 мг в сутки) или индометацином (75 мг в сутки).
Основные группы препаратов,
воздействующих на пуриновый обмен
В настоящее время создан эффективный препарат алломарон, состоящий из аллопуринола (100 мг) и бензбромарона (20 мг), который по эффективности в 2-3 раза превосходит оба компонента. Особенностями алломарона является длительность действия, позволяющая назначать его один раз в сутки (при этом суточная доза аллопуринола составляет всего 100 мг, что снижает риск побочных реакций). Имеются единичные сообщения эффективного плазмафереза и гемосорбции [1, 3].
Урикозурические препараты (пробенецид, сульфинпиразон) в настоящее время не используют в связи с их низкой эффективностью и большим количеством побочных эффектов (риск уратного нефролитиаза).
Дозы гипоурикимических средств подбирают таким образом, чтобы концентрация мочевой кислоты в сыворотке крови не превышала 300мк/моль на литр (5мг/%), так как только в этом случае начнут растворяться кристаллы мочевой кислоты в тканях, а общее ее количество начнет уменьшаться. Это уменьшит повреждение суставов и других органов – приступы подагры прекратятся, исчезнут тофусы, улучшится функция органов, в том числе почек. Урикозурические препараты перестают действовать при снижении СКФ<30мл/мин. Иногда они могут вызвать образование уратных камней, так как повышают концентрацию уратов в моче. Для профилактики камнеобразования назначают обильное питье, ощелачивание мочи, снижают дозу препарата. Аллопуринол – основное средство патогенетического лечения нарушений обмена мочевой кислоты.
Таблица 4. Основные группы препаратов для лечения подагры.
| Урикоингибиторы (урикодепрессивные средства) |
Урикоэлиминаторы (урикозурические средства) |
|
| Механизм | Подавление синтеза мочевой кислоты | Усиление выведения мочевой кислоты почками. |
| Показания | а) метаболический тип подагры с повышенной гиперурикемией (>0,6 ммоль/л), наличием тофусов;
б) подагра с уратной нефропатией (мочекаменной болезнью и др.). В случае почечной недостаточности дозы препаратов уменьшаются не менее чем на 25%; в) смешанный тип подагры при суточной экскреции уратов более 2,7 ммоль (>450 мг). г) вторичная подагра; |
а) почечный тип подагры;
б) отсутствие выраженной подагрической нефропатии; в) возраст моложе 60 лет г) СКФ>80 мл/мин д) суточная экскреция МК<4,8ммоль (800мг) при обычном рационе или 3,6 ммоль (600мг) при ограничении потребления пуринов ж) смешанный тип подагры при суточной экскреции мочевой кислоты менее 2,7 ммоль (<450 мг); з) непереносимость аллопурина. Противопоказаны эти средства: -при метаболическом типе подагры, -при малом объеме выделяемой мочи, — при почечных камнях любого типа. |
| Лечение | Важнейший препарат — аллопуринол. Выпуск — таблетки по 0,1 и 0,3.
Можно начать с 50–100 мг в сутки достигая при легких формах подагры — 200-300 мг в сутки (за 1-2 приема), при более тяжелых — 400-600 мг (2-3 приема). Снижение уровня мочевой кислоты до нормы обычно происходит за 2-3 недели. Далее принимается поддерживающая доза (100-200 мг в сутки). |
а) пробенецид — таблетки по 0,5. начальная доза – 0,25- 0,5 2 раза в день. Затем доза повышается до эффективной (чаще — 1,5-2,0/сутки, т.е. 3-4 таблетки), не более 3,0 в сутки. Действие препарата блокируется при одновременном приеме салицилатов;
б) сульфинпиразон — таблетки по 0,1. суточная доза — 400-600 мг (за 2-3 приема). При достижении эффекта -переходят на поддерживающую дозу (по 100 мг 2-3 раза в день). Обладает дезагрегантным действием (полезно при сочетании подагры с атеросклерозом); в) кетазон — таблетки по 0,25 г. Эффективная доза — 3-4 табл. в день, поддерживающая — обычно 1 таблетка в сутки. |
Таблица 5. Подбор дозы аллопуринола в зависимости от величины СКФ
| СКФ, мл/мин | Доза, мг/сутки |
| > 100 | 300 и более
(при необходимости) |
| 80-100 | 250 |
| 60-80 | 200 |
| 40-60 | 150 |
| 20-40 | 100 |
| 10-20 | 100 мг х 1 р/2 сут. |
| < 10 | 100 мг х 1 р/3 сут. |
Поскольку большинство пациентов с гиперурикемией имеют другие нарушения обменных процессов, в частности гиперлипидемию, гипергликемию, а также артериальную гипертензию, их следует отнести к группе высокого риска сердечно-сосудистых осложнений. В связи с этим им необходимо назначать гиполипидемическую, гипогликемизирующую и антигипертензивную терапию, лечить никотиновую зависимость.
Антигипертензивная терапия: Предпочтение отдается ИАПФ, так как при гиперурикемии активируется локальная почечная ренин-ангиотензиновая система, а также имеются повреждения почек.
Блокаторы рецепторов ангиотензина-2 (БРА) лучше переносятся больными, обладают положительным воздействием на обмен мочевой кислоты, блокируют транспортные системы эпителиоцитов дистальных канальцев почки (урат/лактат, урат/хлорид), снижая в них реабсорбцию уратов, защищая таким образом почечный интерстиций от повреждающего действия уратов, предупреждая развитие и прогрессирование Тубуло-интерстициального нефрита (доказано для лозартана). При этом выведение уратов увеличивается за счет снижения их реабсорбции в канальцах, а не фильтрации в клубочках, таким образом риск нефролитиаза не увеличивается.
Бета-блокаторы и антогонисты кальция метаболически нейтральны и поэтому не влияют на обмен уратов, назначаются больным с гиперурикемией по общепринятым рекомендациям.
Тиазидовые диуретики, широко используемые в качестве антигипертензивных средств, могут провоцировать гиперурикемию у предрасположенных лиц и повышать уровень мочевой кислоты у больных подагрой, поэтому от применения этой группы препаратов у больных с гиперурикемией следует отказаться. В случае ХСН и невозможности отказаться от мочегонных необходим частый мониторинг урикемиии и своевременное присоединение аллопуринола или (по показаниям) применение петлевых диуретиков.
Липиднормализующая терапия: статины.
Гипогликемическая терапия: противодиабетические препараты.
Лечение уратной нефропатии
Мочекаменная болезнь. Для лечения мочекаменной болезни, растворения и предупреждения образования мочекислых и кальций-оксалатных камней, мочекисло-оксалатных камней, для подщелачивания мочи, у пациентов получающих цитостатики или урикозурические препараты рекомендуется Блемарен внутрь, после еды. Средняя суточная доза колеблется от 6 до 18г гранулированного порошка (или 2-6 шипучих таблеток). Суточную дозу делят равномерно на 2-3 приема. Гранулированный порошок или таблетки растворяются в жидкости (1 мерная ложка или 1 табл. на стакан воды, чая, сока или щелочной минеральной воды). Контроль эффективности препарата проводится 3 раза в день перед каждой разовой дозой путем определения рН мочи с помощью индикаторной бумаги. Полученный цвет на бумаге сравнивают в течение 2 мин со шкалой и заносят полученную величину в контрольный календарь. Доза препарата считается правильно подобранной, если рН мочи в течение суток колеблется в пределах 6,2-6,8. Если величина рН ниже 6,2, дозу необходимо увеличить до рН мочи 6,8. Для растворения мочекислых камней величину рН мочи следует поддерживать в пределах 6,2-7,0. Для растворения цистиновых камней значение рН должно быть 7,5-8,5.
Для предотвращения последующего камнеобразования при наличии кальций-оксалатных камней величину рН мочи следует поддерживать от 6,8 до 7,4. На фоне лечения порфирии значение рН должно быть 7,2-7,5, а при лечении цитостатиками – как минимум 7,0. Длительность терапии – от 4 нед до 6 мес. При наличии цистиновых камней и лечении порфирии для контроля эффективности необходимо использовать специальную индикаторную бумагу с величиной рН от 7,2 до 9,7.
Острая мочекислая нефропатия. Заболевание можно предотвратить и при своевременно начатом лечении смертность от него практически равна нулю. В/в введение большого количества жидкости с фуросемидом (до диуреза 100 мл/час) снижает концентрации мочевой кислоты в почечных канальцах предотвращает острую почечную недостаточность. Прием 240 – 500 мг ацетазоламида внутрь каждые 6 – 8 часов и введение бикарбоната (2 ампулы по 44,6 ммоль на 1 литр 5% глюкозы) ощелачивают мочу и увеличивают растворимость мочевой кислоты. Для уменьшения притока мочевой кислоты в почки назначают аллопуринол 8мг/кг, если функция почек не восстанавливается дозу снижают до 100 – 200 мг/сут. Важно не допускать гиповолемии и снижения Ph мочи ниже 7. При неэффективности консервативных мероприятий – гемодиализ.
Хронический тубуло-интерстициальный нефрит (ХТИ) – коррекция гиперурикемии, гипергликемии (при ее наличии), гиперлипидемии (при ее наличии), антигипертензивная терапия.
Физиотерапевтическое лечение
Таблица 6. Физиотерапевтическое лечение при подагре.
| Острый приступ суставной подагры |
Межприступный период хронической артропатии |
|
|
Фитотерапия подагры
Рекомендуется следующий сбор: трава зверобоя, цветки ромашки, липы и черной бузины (в равных количествах) – в виде настоя (15,0-200,0) – по 2 стакана в день.
В связи с успехами комплексной терапии подагры современные исследователи находят возможность относить ее «к тем благодарным болезням, раннее распознавание которых позволяет сохранить здоровье человека на многие годы».
Что же касается ее раннего распознавания, то ободряюще звучит мысль И.Мадьярова: «отличить подагру от иных заболеваний суставов обычно нетрудно, но только в том случае, если при любом суставном заболевании помнить о ней».
Гипоурикемия
Гипоурикемия – концентрация мочевой кислоты в сыворотке менее 120 мкмоль/л (2 мг%) – возникает при замедлении образования мочевой кислоты, усилении ее экскреции или сочетании этих причин. Гипоурикемию выявляют менее чем у 0,2% населения в целом и менее чем у 0,8% больных в стационарах. Гипоурикемия сама по себе безвредна и не требует лечения, но может быть проявлением какой-либо болезни, поэтому нужно обязательно выяснить ее причину.
Наиболее частая причина гипоурикемии — относительное увеличение экскреции мочевой кислоты. Неизмененная суточная экскреция мочевой кислоты при гипоурикемии свидетельствует о нарушении функции почек. Некоторые лекарственный средства, например аспирин в дозе более 2 г/сут, контрастные вещества и гвайфенезин, обладают урикоурическим действием:
Таблица 7. Препараты снижающие урикемию.
| Аскорбиновая кислота
Бензбромарон Глюкокортикоиды Дикумарол Контрастные вещества Кортикотропин Меклофенамовая кислота Салицилаты (> 2 г/сут) Хлорпротиксен Цитраты Эстрогены |
Врожденные нарушения пуринового обмена
Таблица 7. Врожденные причины подагры.
| Фермент | Нарушение | Тин наследования | Клиническая картина |
| Гипоксантинфосфорибозилтрансфераза | отсутствие фермента | х-сцепленный рецессивный | Агрессивное поведение, склонность к самоповреждению, хореоатетоз, гиперурикемия, подагра и уратные мочевые камни |
| недостаточность | х-сцепленный рецессивный | Гиперурикемия, подагра и уратные мочевые камни | |
| Фосфорибозилпирофосфатснтетаза | избыточная активность | х-сцепленный рецессивный | Гиперурикемия, подагра, уратные мочевые камни и глухота. |
| Аденинфосфорибозилтрансфераза | недостаточность | аутосомно-рецессивный | Мочевые камни, состоящие из 2,8-дигидроксиаденина |
| Ксантиноксидаза | недостаточность | аутосомно-рецессивный | Ксантинурия и ксантиновые мочевые камни |
| Аденилосукцинатлиаза | недостаточность | аутосомно-рецессивный | Аутизм и психомоторная заторможенность |
| АМФ-дезаминаза | недостаточность | аутосомно-рецессивный | Бессимптомное течение или миопатии с непереносимостью физической нагрузки |
| Аденозиндезаминаза | недостаточность | аутосомно-рецессивный | Комбинированный иммунодефицит, иногда с нарушением развития скелета |
| Пуриннуклеозидфосфорилаза | недостаточность | аутосомно-рецессивный | Недостаточность клеточного иммунитета |
Литература
- Барскова В.Б., Якунина И.А.. Противовоспалительная терапия острого и хронического подагрического артрита. Справочник поликлинического врача 2006;2: 90-94.
- Крякунов К.Н.. Диагностика и лечение подагры. Санкт-Петербургские врачебные ведомости 1994;2:21-27.
- Вортман Р.. Нарушения пуринового обмена. Внутренние болезни по Тинсли Р.Харрисону, т.2. 2002; 2612-2626.
- Мухин Н.А.. Подагра – только ли болезнь суставов? Клиническая фармакология и терапия. 1994; 1: 31-33.
- Барскова В.Г. Метаболический синдром и кардиоваскулярные нарушения при подагре. Автореферат дис. д.м.н. М 2006.
- Клинические разборы под ред. Н.А. Мухина, подагрическая почка, М. Литтерра, 2005; 237-261.
- Портнягин В.Ф. Подагра. Учебное пособие. 2006.