АКРОМЕГАЛИЯ — Медицинский справочник
Содержание страницы
Определение
Акромегалия (от греч. akros — «крайний», megas — «большой») относится к группе нейроэндокринных заболеваний, обусловленных патологическим повышением ростовой активности.
В детском и юношеском возрасте (до окончания окостенения эпифизарных хрящей) при чрезмерной ростовой активности развивается гигантизм. После закрытия ростовых зон он переходит в акромегалию. Гигантизм характеризуется сравнительно пропорциональным эпифизарным и периостальным увеличением костей, мягких тканей и внутренних органов. При акромегалии, напротив, увеличение костей скелета в периостальной зоне и внутренних органов отличается диспропорциональностью; кроме того, развивается ряд обменных нарушений.
Акромегалия является редким заболеванием и развивается преимущественно у взрослых.
Этиология и патогенез
Основную роль в развитии акромегалии играет увеличение секреции соматотропного гормона гипофиза — гормона роста. Наиболее частой причиной гиперпродукции соматотропина является гормонально-активная аденома (см.) гипофиза — соматотропинома. Несколько реже встречается первичное поражение гипоталамуса или вышерасположенных отделов мозга. К нему могут приводить травмы черепа с сотрясением мозга, психоэмоциональные нагрузки, внегипофизарные опухоли головного мозга, влияние на центральную нервную систему специфических и неспецифических инфекционных процессов. При этом увеличивается синтез соматолиберина, а уже вслед за тем опосредованно — синтез соматотропина. К возникновению акромегалии может приводить повышенная активность соматомединов, которые вырабатываются печенью и периферическими тканями в ответ на воздействие соматотропина, а также повышенная чувствительность тканей к ним. Это связано с тем, что соматомедины оказывают непосредственное влияние на рост костно-суставного аппарата. Кроме того, акромегалия как синдром может развиваться при наличии эктопической продукции соматотропина или соматолиберина опухолями неэндокринной локализации (легкие, желудок, кишечник и др.). На возникновение акромегалии способны также влиять резкие колебания гормонального фона, что особенно характерно для женского организма: роды (см.), аборты (см.), климактерический (см.) и посткастрационный периоды.
Клиническая картина
В течении акромегалии выделяют ряд стадий. Заболевание развивается годами. В связи с этим наиболее ранняя стадия — преакромегалическая — выявляется достаточно редко, поскольку симптоматика не столь отчетлива, как на гипертрофической стадии. Гипертрофическая стадия характеризуется развернутой клиникой заболевания. Типичны жалобы на головную боль, изменение внешности, увеличение в размерах кистей и стоп. Кроме того, пациентов беспокоят онемение в руках, слабость, сухость во рту, жажда, боль в суставах, ограничение и болезненность движений. У большинства женщин развиваются нарушения менструального цикла вплоть до аменореи (см.), у трети больных (мужчин) развивается импотенция (см.). При сочетании гиперпродукции соматотропина и пролактина отмечается синдром галактореи (см.).
Головные боли беспокоят преимущественно при опухолевой природе акромегалии. Их связывают с повышением внутричерепного
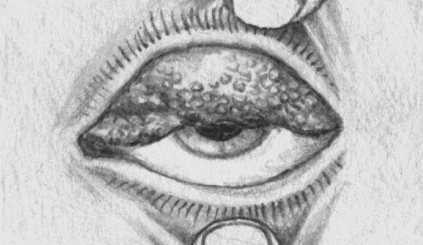
давления и (или) компрессией растущей аденомой диафрагмы турецкого седла. К изменениям внешности приводит огрубение черт лица, связанное с увеличением надбровных дуг, скуловых костей, нижней челюсти. Расширяются межзубные промежутки (диастема). Кроме того, характерна гипертрофия мягких тканей лица — носа, губ, ушей. Увеличивается язык (макроглоссия), на котором сохраняются отпечатки зубов.
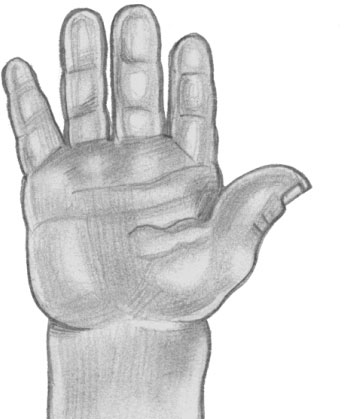
Кисть больного акромегалией
Довольно часто при акромегалии отмечаются изменения со стороны кожных покровов: гиперпигментация (чаще в области кожных складок и мест трения одеждой), повышенная жирность и влажность благодаря увеличению количества и размеров потовых и сальных желез, лихенизация (см.) и складчатость (более выражены на волосистой части головы). Отмечается также гипертрихоз (см.).
Изменения со стороны мышц заключаются не столько в гипертрофии мышечной ткани, сколько в разрастании соединительнотканных структур. В начале заболевания отмечается повышение мышечной силы и работоспособности пациентов, однако по мере его прогрессирования мышечные волокна подвергаются склерозированию, развивается проксимальная миопатия. Гипертрофия хрящевой ткани в суставах приводит к появлению акромегалической артропатии. В результате пролиферации хрящей гортани голос у больных становится низким и сиплым.
На начальных этапах заболевания увеличенные внутренние органы функционируют нормально. Но вследствие прогрессирования болезни присоединяются признаки сердечной, легочной и печеночной недостаточности. Быстрее, чем в норме, возникают атеросклеротические изменения сосудов, развивается повышение артериального давления. Сердце увеличивается в размерах за счет разрастания соединительной ткани и гипертрофии мышечных волокон, однако клапанный аппарат при этом не изменяется, что приводит к развитию недостаточности кровообращения. На стадии развернутых клинических проявлений характерна миокардиодистрофия (см.), возможно нарушение внутрисердечной проводимости.
У трети всех больных отмечаются акропарестезии разной степени выраженности, которые появляются в результате сдавления нервов разросшимися костными структурами или мягкими тканями.
Обменные нарушения связаны с патологическим влиянием гиперпродукции соматотропина. Для них характерны активация процессов липолиза, увеличение окисления жиров в периферических тканях, повышение содержания в сыворотке крови холестерина, кетоновых тел, бета-липопротеидов, лецитина, неэстерифицированных жирных кислот (причем чем больше последних, тем активнее течение заболевания). У 50—60% пациентов наблюдаются нарушения устойчивости к глюкозе, а явный сахарный диабет (см.) развивается у 1/5 больных. Соматотропин является контринсулярным гормоном. Его биологическое влияние на углеводный обмен сводится к стимуляции глюконеогенеза, снижению утилизации глюкозы мышечной тканью. Он также обладает способностью угнетать активность гликолитических ферментов периферических тканей за счет липолитического действия гормона и высокого уровня свободных жирных кислот.
Нарушения минерального обмена связаны с воздействием соматотропина на функциональную активность почек. Он усиливает экскрецию с мочой кальция, калия, натрия, хлоридов. Характерны для акромегалии нарушения фосфорно-кальциевого баланса.
При акромегалии, связанной с развитием аденомы гипофиза (см.), наступает период появления офтальмоневрологической симптоматики, связанной с ростом опухоли за пределы турецкого седла. Сдавление области перекреста зрительных нервов проявляется битемпоральной гемианопсией, снижением остроты и сужением полей зрения. На глазном дне отмечается последовательная смена отека, стаза и атрофии зрительных нервов. При отсутствии лечения это приводит к слепоте.
Рост опухоли преимущественно в сторону гипоталамуса вызывает у больных сонливость, жажду, полиурию, резкие подъемы температуры. Преимущественно фронтальный рост приводит к возникновению эпилепсии, поражение обонятельного тракта — к аносмии. Врастание опухоли в области кавернозных синусов характеризуется поражением III, IV, V и VI пар черепно-мозговых нервов. Клинически это проявляется в птозе, офтальмоплегии, диплопии, лицевой анальгезии, снижении остроты слуха. Кроме того, возникают или усиливаются признаки внутричерепной гипертензии (см.).
Исходом заболевания является кахексия.
При отсутствии соответствующего лечения, при неблагоприятном течении и раннем начале (в молодом возрасте) продолжительность жизни больных составляет 3—4 года. При медленном развитии и благоприятном течении человек может прожить от 10 до 30 лет. При своевременном лечении прогноз для жизни благоприятный, возможно выздоровление. Трудоспособность ограничена.
Диагностика
В диагностике, помимо физикального, обследования и анамнестических данных доминирующее значение придается рентгенологическим и биохимическим методам.
При рентгенографии костей скелета отмечаются явления периостального гиперостоза с признаками остеопороза (см.). На рентгенограммах черепа просматривается истинный прогнатизм, расхождение зубов, увеличение затылочного бугра и утолщение свода черепа. Нередко отмечается кальцификация твердой мозговой оболочки. В 70—90% случаев увеличены размеры турецкого седла. С помощью компьютерной или ЯМР-томографии можно увидеть и саму аденому.
Среди лабораторных методов достаточно информативным является определение концентрации соматотропина в крови радиоиммунологическим методом. При этом о гиперсекреции свидетельствует стойкое превышение нормального уровня гормона (7—10 мкг/л). Кроме того, при акромегалии отмечается изменение физиологической секреции соматотропина в ответ на стандартный глюкозотолерантный тест, внутривенное введение тиреолиберина — парадоксальное повышение концентрации гормона роста. В начальной стадии сна, напротив, уровень соматотропина не изменяется. При проведении тестов с инсулиновой гипогликемией (см.), L-Допа, допамином и бромокриптином, а также при физической нагрузке отмечается парадоксальное снижение концентрации гормона.
Акромегалию следует дифференцировать с пахидермопериостозом, болезнью Реджета и синдромом Мари—Бамбергера.
Лечение
Лечение акромегалии включает в себя комплекс мер, направленных на снижение концентрации соматотропина в сыворотке крови. При опухолевой природе заболевания у молодых больных предпочтительнее оперативное вмешательство с последующей лучевой терапией. Если позволяют размеры аденомы (не выходит за пределы турецкого седла), операцию проводят с использованием транссфеноидального доступа для минимальной травматизации окружающих тканей. При значительных размерах аденомы проводится трансфронтальная аденомэктомия. Показаниями к такому оперативному вмешательству являются прогрессирующее сужение полей зрения, неврологические нарушения, упорные головные боли, подозрение на злокачественное новообразование.
Дистанционное лучевое воздействие на промежуточно-гипофизарную область проводят рентгеновскими и гамма-лучами, а также направленным протонным пучком. Последний способ предпочтительнее в связи с большей эффективностью. Используются дозы от 4,5 до 15 тыс. рад в зависимости от размеров опухоли. Если оперативное лечение невозможно, эффект от изолированно применяемой лучевой терапии наступает спустя 1—2 года после облучения.
Признаками стабилизации процесса являются исчезновение потливости, снижение отечности, нормализация показателей артериального давления и углеводного обмена. Объективным критерием является снижение уровня концентрации соматотропина в сыворотке крови.
У пожилых пациентов при невозможности хирургического и лучевого лечения применяются медикаментозные препараты группы стимуляторов допаминергических рецепторов (бромокриптин, лисенил-форте), которые способны тормозить секрецию соматотропина. На размеры аденомы они влияния не оказывают. Суточная дозировка бромокриптина составляет от 10 до 20 мг. Эффект наступает спустя 2—3 недели после начала лечения и сохраняется только в период приема препарата.
В комплексной терапии в связи с многочисленными обменными нарушениями и осложнениями следует использовать симптоматические средства. Больные нуждаются в соответствующей диете с ограничением поваренной соли (не более 5 г в сутки), жиров и легкоусвояемых углеводов. При развитии сахарного диабета следует принимать сахароснижающие средства или использовать инсулин. После аденомэктомии или лучевого лечения больные могут нуждаться в назначении заместительной терапии гормонами надпочечников или щитовидной железы.