Ревматоидный артрит
Содержание страницы
Ревматоидный артрит (РА)- воспалительное ревматическое заболевание неизвестной этиологии, характеризующееся симметричным хроническим эрозивным артритом (синовитом) периферических суставов и системным воспалительным поражением внутренних органов.
1. Эпидемиология
РА — одно из наиболее распространённых хронических воспалительных заболеваний человека, частота которого в популяции в среднем составляет 1%. Болезнь встречается примерно в 2,5 раза чаще у женщин, чем у мужчин, однако у пациентов, серопозитивных по ревматоидному фактору (РФ), и у лиц пожилого возраста эти половые различия менее очевидны.
2. Этиология
Этиология РА неизвестна.
Генетическая предрасположенность
Риск заболеть РА увеличен (примерно в 16 раз) у кровных родственников больных. Конкордантность у монозиготных близнецов колеблется от 15 до 30%, что в 4 раза выше, чем у дизиготных близнецов. Это свидетельствует об участии нескольких генов в реализации генетической предрасположенности к заболеванию. Имеются данные о связи между развитием РА и носительством определённых аллелей Аг HLA класса II, а именно полиморфизмом HLA-DR4 (особенно эпитопа DRB1). У носителей HLA-DR4 чаще наблюдают тяжёлое течение заболевания и серопозитивность по РФ.
Гормональные нарушения
О роли гормонов (половые гормоны, пролактин) свидетельствует тот факт, что в возрасте до 50 лет РА наблюдают примерно в 2-3 чаще у женщин, чем у мужчин, а в более позднем возрасте эти различия нивелируются. У женщин приём пероральных контрацептивов и беременность снижают риск развития РА, а в послеродовом периоде во время кормления грудью (гиперпролактинемия) риск заболеть существенно увеличивается.
3. Патогенез
Суть патологического процесса при РА — генерализованное, иммунологически обусловленное (аутоиммунное) воспаление, приводящее к развитию широкого спектра внесуставных (системных) органных проявлений и катаболических нарушений (например, остеопороз).
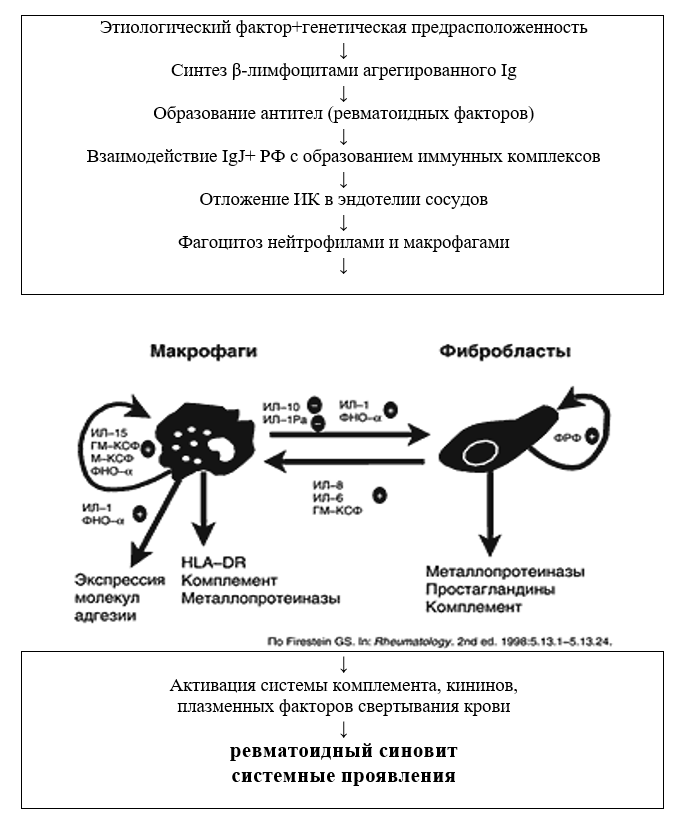
Рисунок. Патогенез ревматоидного артрита.
4. Патоморфология
Суставы. Формируются лимфоидные фолликулы. В большом количестве обнаруживают плазматические клетки, пролиферацию кроющих синовиоцитов типа В. В перихондральной части синовиальной мембраны происходит формирование паннуса, хрящ под паннусом истончён, с глубокими трещинами. В субхондральной пластинке кости обнаруживают множественные эрозии. Остеокласты крупные, расположены неравномерно. Деструктивные процессы в кости сочетаются с врастанием в зону обызвествления сосудов и паннуса.
Сосуды. Поражение сосудов микроциркуляторного русла представлено васкулитами и ангиоматозом, утолщением базальных мембран капилляров и венул. На поздних стадиях развивается ангиоматоз в сочетании с продуктивными васкулитами и тромбозами.
Ревматоидный узелок — очаг фибриноидного некроза, окружённый палисадо-образно расположенными макрофагами, плазматическими клетками, лимфоцитами с нередким присутствием гигантских многоядерных клеток.
Мышцы — очаговый или диффузный миозит, продуктивные васкулиты, локальный фиброз.
Сердце — неспецифические экссудативно-пролиферативные реакции, поражение мышечных волокон дистрофического характера, проявления васкулита.
Серозные оболочки — изменения серозных оболочек (перикардит, плеврит). Особенности перикардита — участие в воспалении крупных базофильных гистиоцитов, образование зоны грануляционной ткани, содержащей лимфоциты и плазматические клетки.
Лёгкие — хроническая интерстициальная пневмония, очаговый или диффузный пневмосклероз.
Почки — мембранозный или мезангиальный гломерулонефрит, нефроангиосклероз, интерстициальный нефрит, амилоидоз
ЖКТ — изменения в ЖКТ возможны на всём его протяжении (гастрит, колит, гепатит), хотя и не доминируют в клинической картине.
5. Классификация
(Ассоциация ревматологов России, 2007)
1.Основной диагноз:
- Ревматоидный артрит серопозитивный (М05.8)
- Ревматоидный артрит серонегативный (М06.0)
- Особые клинические формы ревматоидного артрита:
— Синдром Фелти (М05.0)
— Болезнь Стилла, развившаяся у взрослых (M06.1)
— Ревматоидный артрит вероятный (М05.9, М06.4, М06.9)
2. Клиническая стадия:
- Очень ранняя стадия: длительность болезни <6 месяцев
- Ранняя стадия: длительность болезни 6 мес. — 1 год
- Развернутая стадия: длительность болезни >1 года при типичной симптоматике РА
- Поздняя стадия: длительность болезни 2 года и более + выраженная деструкции мелких (III-IV рентгенологическая стадия) и крупных суставов, наличие осложнений
3. Активность болезни:
0 = ремиссия (DAS28 < 2,6)
1 = низкая (2,6< DAS28 <3,2)
2 = средняя (DAS28 3,2 — 5,1)
3 = высокая (DAS28 > 5,1)
4. Внесуставные (системные) проявления:
- ревматоидные узелки
- кожный васкулит (язвенно-некротический васкулит, инфаркты ногтевого ложа, дигитальный артериит, ливедо-ангиит)
- васкулит других органов
- нейропатия (мононеврит, полинейропатия)
- плеврит (сухой, выпотной), перикардит (сухой, выпотной)
- синдром Шегрена
- поражение глаз (склерит, эписклерит, васкулит сетчатки)
5. Инструментальная характеристика:
- Наличие эрозий (с использованием рентгенографии, возможно МРТ, УЗИ):
- Неэрозивный
- Эрозивный
- Рентгенологическая стадия (по Штейнброкеру, модификация):
- I — околосуставной остеопороз
- II – остеопороз + сужение суставной щели, могут быть единичные эрозии
- III – признаки предыдущей стадии + множественные эрозии + подвывихи в суставах
- IV – признаки предыдущей стадии + костный анкилоз
6. Дополнительная иммунологическая характеристика – антицитруллиновые анти-тела:
- АЦЦП – позитивный
- АЦЦП – негативный
7.Функциональный класс:
- I – полностью сохранены: самообслуживание, непрофессиональная и профессиональная деятельность
- II – сохранены: самообслуживание, профессиональная деятельность, ограничена: непро-фессиональная деятельность
- III – сохранено: самообслуживание, ограничены: непрофессиональная и профессио-нальная деятельность
- IV – ограничены: самообслуживание, непрофессиональная и профессиональная деятель-ность
8. Осложнения:
- вторичный системный амилоидоз
- вторичный артроз
- остеопороз (системный)
- остеонекроз
- туннельные синдромы (синдром карпального канала, синдромы сдавления локтевого, большеберцового нервов)
- подвывих в атланто-аксиальном суставе, в том числе с миелопатией, нестабильность шейного отдела позвоночника
- атеросклероз
Серопозитивность и серонегативность РА определяются по тесту на ревматоидный фактор, который должен быть проведен с использованием достоверного количественного или по-луколичественного теста (латекс-тест, иммуноферментный метод, ммунонефелометрический метод).
В качестве базового метода оценки активности рекомендуется применять индекс DAS28 = 0,56√ЧБС+0,28√ЧПС+0,70lnСОЭ+0, 014ООСЗ,
где ЧБС – число болезненных суставов, ЧПС – число припухших суставов (плечевые, локтевые, лучезапястные, пястнофаланговые, проксимальные межфаланговые, коленные), СОЭ, ООСЗ – общая оценка больным состояния здоровья по 100–иллиметровой визуальной аналоговой шкале.
Примеры формулировки клинических диагнозов:
- Ревматоидный артрит серопозитивный (М05.8), развернутая стадия, активность II, эрозивный (стадия II), с системными проявлениями (ревматоидные узелки), АЦЦП (-), ФК II.
- Ревматоидный артрит серонегативный (М06.0), ранняя стадия, активность III, неэрозивный (стадия I), АЦЦП (+), ФК I.
- Ревматоидный артрит серопозитивный (М05.8), поздняя стадия, эрозивный (стадия III), активность II, с системными проявлениями (склерит, дигитальный артериит), ФК III.
Осложнения: Амилоидоз почек, ХБП III.
- Вероятный ревматоидный артрит (М06.9), серонегативный, ранняя стадия, активность II, неэрозивный (стадия I), АЦЦП (+), ФК I.
6. Клиническая картина
Общие проявления
Характерный признак заболевания — ухудшение общего состояния (ощущение генерализованной слабости, скованности, особенно в утренние часы, артралгии, похудание, субфебрильная температура тела, лимфаденопатия), которое может предшествовать клинически выраженному поражению суставов.
Поражение суставов
Изменения суставного статуса, с которыми приходится сталкиваться при обследовании больных, складываются из трех основных компонентов. Это, прежде всего признаки воспаления синовиальной оболочки самого сустава. Второй компонент – это патология околосуставных мягких тканей, которая может быть проявлением воспаления (бурсит, тендинит, тендовагинит), фиброза, ведущего к формированию контрактур и анкилозов, и недостаточности связочного аппарата с возникновением подвывихов. Наконец, третья составляющая суставного статуса – деструкция хряща и костей.
Обычно деструктивные изменения оцениваются по рентгенограммам. Грубая деструкция ведет к деформации сустава, которую можно обнаружить при осмотре. Примерно в половине случаев заболевание начинается с постепенного (в течение месяцев) нарастания болей и скованности в мелких периферических суставах (лучезапястных, проксимальных межфаланговых, пястно-фаланговых, голеностопных и плюснефаланговых). Иногда заболевание дебютирует как острый моноартрит крупных суставов, напоминающий септический или микрокристаллический артрит, или начинается с рецидивирующих бурситов и тендосиновитов, особенно часто локализующихся в области лучезапястных суставов, приводя к развитию синдрома запястного канала. У лиц пожилого возраста заболевание может начинаться с острого полиартрита с множественным поражением мелких и крупных суставов, с генерализованной полиартралгии или симптомов, напоминающих ревматическую полимиалгию.
Поражение суставов
Наиболее частый и характерный признак воспаления синовиальной оболочки суставов при РА — утренняя скованность. Её длительность обычно тесно связана с выраженностью синовита и составляет не менее 1 ч.
В дебюте заболевания клинические проявления могут быть выражены умеренно и часто носят субъективный характер. Только у некоторых больных с очень активным течением заболевания выявляют классические признаки воспаления суставов, такие, как повышение температуры кожи и отёк суставов (чаще коленных, реже проксимальных межфаланговых и запястья). Для большинства пациентов характерно симметричное поражение суставов кистей (проксимальных межфаланговых, пястно-фаланговых и лучезапястных), а также плюснефаланговых суставов. Крайне характерно вовлечение в процесс коленных, голеностопных, плечевых, локтевых и тазобедренных суставов, а также шейного отдела позвоночника. Поражение суставов, как правило, связано с вовлечением связочного аппарата, приводя к гипермобильности и деформации суставов на более поздних стадиях болезни.
Кисть
Ульнарная девиация пястно-фаланговых суставов (развивается через 1-5 лет от начала болезни), поражение пальцев кисти по типу «бутоньерки» (сгибание в проксимальных межфаланговых суставах) или «шеи лебедя» (переразгибание в проксимальных межфаланговых суставах), деформации по типу «лорнетки».
Коленные суставы
Сгибательная и вальгусная деформация; киста Бейкера.
Стопы
Подвывихи головок плюснефаланговых суставов, латеральная девиация, деформация большого пальца.
Шейный отдел позвоночника
Подвывихи в области атлантозатылочного сочленения, изредка осложняются компрессией спинного мозга или позвоночной артерии.
Перстневидно-черпаловидный сустав
Огрубение голоса, одышка, дисфагия, рецидивирующий бронхит.
Поражение связок
Тендосиновит в области лучезапястного сустава и кисти (боль, отёк, нарушение функции, сгибательные контрактуры).
Бурсит
Бурсит: чаще всего в области локтевого сустава. Синовиальная киста на задней стороне коленного сустава (киста Бейкера), сопровождающаяся повышением давления в коленном суставе (может привести к разрыву с болями в икроножных мышцах, отёку голеностопного сустава, что необходимо дифференцировать с тромбозом глубоких вен голени).
Внесуставные проявления
Поскольку РА — системное заболевание, у многих больных возникают различные внесуставные проявления, некоторые из которых наблюдают уже в дебюте заболевания и могут (хотя и очень редко) превалировать в клинической картине болезни. Факторы риска развития системных проявлений: тяжёлое поражение суставов, высокие титры РФ и, вероятно, экспрессия аллеля HLA-DRB 1*0401.
Ревматоидные узелки
Ревматоидные узелки выявляют у 20-50% больных РА. Они наиболее часто локализуются поверхностно в местах, подверженных механическому сдавлению (в области сумки и вдоль сухожилий локтевого отростка, ахиллова сухожилия, над мелкими суставами кистей), очень редко — в ткани висцеральных органов.
Поражение лёгких
На аутопсии признаки поражения лёгких выявляют у половины больных РА. Однако клинически значимую патологию (плеврит, интерстициальный лёгочный фиброз, неотличимый от идиопатического, облитерирующий бронхиолит, ревматоидные узелки в лёгком, лёгочный васкулит) наблюдают реже, обычно у больных с тяжёлым серопозитивным РА. Кроме того, патология лёгких может быть связана с приёмом многих базисных противоревматических препаратов (метотрексат, D-пеницилламин, соли золота). В целом, смертность больных РА от лёгочной недостаточности в 2 раза выше, чем в общей популяции.
Поражение сердца
Поражение сердца связано с различными формами патологии, в том числе с васкулитом, образованием узелков, амилоидозом, серозитом, вальвулитом и фиброзом, и чаще встречается при тяжёлом течении заболевания. Наибольшее клиническое значение имеет перикардит (сухой, реже выпотной). Необходимо учитывать, что больные РА склонны к раннему развитию атеросклеротического поражения сосудов.
Поражение глаз
Наиболее частое офтальмологическое проявление РА — сухой кератоконъюнк-тивит, развивающийся в рамках вторичного синдрома Шёгрена, часто выявляемый только при специальном офтальмологическом обследовании. Нередко наблюдают эпизоды эписклерита и склерита. Описано развитие склеромаляции, связанной с образованием ревматоидных узелков в области склеры.
Поражение нервной системы
Поражение нервной системы включает компрессионную невропатию (туннельные синдромы), симметричную сенсорно-моторную невропатию и множественный мононеврит. Невропатия — характерное проявление ревматоидного васкулита. Тяжёлым, хотя и очень редким, осложнением является цервикальная миелопатия, связанная с подвывихом в области атлантозатылочного сочленения.
Поражение мышц
Поражение мышц проявляется мышечной слабостью, обычно связанной с мышечной атрофией, возникающей на фоне воспаления суставов, или периферической невропатией. Воспалительная миопатия развивается очень редко, уровень КФК обычно в норме или умеренно повышен. Необходимо принимать во внимание возможность развития синдрома миопатии на фоне лечения D-пеницилламином, невро- или миопатии на фоне лечения антималярийными препаратами и миопатии, индуцированной глюкокортикоидами.
Поражение почек
Поражение почек, обусловленное самим РА, редко клинически значимо. При биопсии почек могут выявляться признаки мезангиального гломерулонефрита и очень редко мембранозной нефропатии. Иногда наблюдают развитие нефротического синдрома, связанного с вторичным амилоидозом или приёмом базисных противоревматических препаратов (соли золота, D-пеницилламин). Амилоидоз развивается преимущественно у больных с длительно текущим РА с высокой воспалительной активностью. Наиболее характерный признак амилои-доза — развитие стойкой протеинурии, позднее нефротического синдрома.
Ревматоидный васкулит
Клинически выраженный системный ревматоидный васкулит относится к числу редких осложнений РА и обнаруживается менее чем у 1% больных, но на аутопсии признаки воспалительного поражения сосудов выявляют почти в четверти случаев. Ревматоидный васкулит чаще развивается у мужчин с тяжёлым серопозитивным РА. Классические клинические признаки ревматоидного васкулита — периферическая гангрена и компрессионная невропатия (множественный мононеврит, дистальная симметричная сенсорная или сенсорно-моторная невропатия), реже склерит, перикардит и поражение лёгких, инфаркты околоногтевого ложа (дигитальный артериит), кожная сыпь, хронические язвы голени. Практически у всех больных имеют место тяжёлые общие симптомы и выявляются ревматоидные узелки.
Синдром Фелти
Синдром Фелти — симптомокомплекс, проявляющийся выраженной нейтропе-нией, спленомегалией, тяжёлым поражением суставов, системными прояв-лениями (васкулит, невропатия, лёгочный фиброз, гепатомегалия, синдром Шёгрена), гиперпигментацией кожи нижних конечностей и высоким риском инфекционных осложнений. У больных с синдромом Фелти в 12 раз увеличен риск развития неходжкенской лимфомы.
Синдром Шёгрена
Синдром Шёгрена — аутоиммунная экзокринопатия (аутоиммунный эпителит), наиболее часто встречается при РА, реже — при других системных заболеваниях соединительной ткани (например, при системной красной волчанке, полимиозите, системной склеродермии). В качестве самостоятельной формы выделяют первичный синдром Шёгрена, не связанный с определённым ведущим заболеванием. К основным клиническим проявлениям синдрома Шёгрена относят сухой кератоконъюнктивит (ощущение зуда, жжения, дискомфорта, позднее снижение остроты зрения, рези, «песка в глазах») и ксеростомию (сухость во рту).
7. Диагностика
Общий анализ крови
Частые лабораторные признаки РА — острофазные реакции (гипохромная анемия, увеличение СОЭ и С реактивного белка). Исследование СОЭ и СРВ важно не только для дифференциальной диагностики РА от невоспалительных заболеваний суставов, но и для оценки активности воспаления, эффективности терапии и прогноза. Другие лабораторные нарушения, такие, как гипергам-маглобулинемию, гипокомплементемию, тромбоцитоз и эозинофилию, обычно выявляют у пациентов с тяжёлым течением РА, а нейтропению — при синдроме Фелти. Иногда наблюдают увеличение уровня печёночных ферментов, связанное с активностью заболевания.
Иммунологические исследования
Среди лабораторных методов значение для диагностики РА имеет определение РФ класса IgM, который в целом выявляют у 70-90% больных. Высокие титры РФ коррелируют с тяжестью, быстротой прогрессирования патологического процесса и развитием системных проявлений, но динамика титров не отражает эффективность проводимой терапии. У здоровых лиц пожилого возраста наблюдают повышение частоты выявления РФ, поэтому диагностическая значимость этого теста для диагностики РА в пожилом возрасте снижается. Необходимо иметь в виду, что в первые 3 мес заболевания РФ выявляют примерно у 30%, а в первые 6 мес — у 60% больных РА, а примерно 12% пациентов (обычно пожилого возраста; чаще мужчины, чем женщины) в течение длительного времени остаются серонегативными. Таким образом, определение РФ не является «идеальным» методом ранней диагностики РА.
У больных синдромом Шёгрена выявляют высокие титры РФ и антинуклеарного (АНФ) факторов, AT к Ro/La и широкому спектру органоспецифических аутоантигенов (париетальные клетки желудка, щитовидная железа, гладкая мускулатура, митохондрии и др.). С очень высокой частотой возникает криоглобулинемия, обычно смешанная моноклональная (тип II), с РФ моноклонального типа IgMк.
Анализ синовиальной жидкости
Анализ синовиальной жидкости имеет вспомогательное значение и используется главным образом при дифференциальной диагностике РА с другими заболеваниями суставов (остеоартроз, микрокристаллические и септический артриты). Для РА (как и других воспалительных артритов) характерны снижение вязкости, рыхлый муциновый сгусток, лейкоцитоз (более 6 * 109/л) с нейтрофилёзом (25-90%).
Рентгенологическое исследование
Рентгенологическое исследование суставов кистей и стоп имеет определяющее значение для диагностики и оценки прогрессирования РА. Характерных изменений в других суставах (по крайней мере, на ранних стадиях болезни) не наблюдается. Ранний рентгенологический признак РА — околосуставной остеопороз, выявляемый уже в первые месяцы болезни, коррелирующий с активностью болезни, нечёткость контуров суставов (при наличии выпота).
Более характерно образование эрозий (или узур) на суставных поверхностях. Эрозии наиболее рано образуются в области головок пястно-фаланговых и плюснефаланговых суставов (головка V плюсневой кости) даже в отсутствие клинических признаков РА. Иногда развиваются обширные разрушения (остеолиз) суставных поверхностей, вплоть до полного исчезновения головок костей мелких суставов кистей и стоп. Параллельно отмечают сужение суставных щелей, вплоть до их исчезновения (анкилоз) и подвывихи в пястно-фаланговых и плюснефаланговых суставах с отклонением в латеральную сторону.
Артроскопия
Артроскопия в сочетании с синовиальной биопсией на ранней стадии не позволяет чётко дифференцировать РА от других воспалительных заболеваний суставов, однако характер морфологических изменений может иметь определённое прогностическое значение.
Тест Ширмера
Тест Ширмера используют для выявления сухого кератоконъюнктивита — характерно снижение слезоотделения после стимуляции (10 мм от метки специальной бумажной полоски в течение 5 мин); окраску эпителия конъюнктивы и роговицы бенгальским розовым или флюоресцеином с последующей биомикроскопией.
Сиалография
Для диагностики паренхиматозного паротита используют сиалографию. Важное значение имеет биопсия слизистой оболочки нижней губы, позволяющая выявить раннее поражение слюнных желёз, ещё до развития клинических проявлений ксеростомии: лимфоцитарная инфильтрация (более 1 очага, состоящего более чем из 50 лимфоцитов) подтверждает диагноз синдром Шёгрена.
Ранняя диагностики РА: определение антител к цитруллину (увеличивает долю ранней диагностики РА на 15-20 %), магнитно-резонансная томография (МРТ) — на ранних стадиях, когда обычная рентгеновская диагностика бессильна, МРТ позволяет увидеть отек костной ткани, а иногда и мельчайшие эрозии. Иногда МРТ дает возможность поставить диагноз уже через месяцы после начала заболевания.
8. Критерии диагноза
Для постановки диагноза РА необходимо наличие по крайней мере четырёх из семи критериев, предложенных Американской коллегией ревматологов. Признаки 1-4 должны устойчиво сохраняться не менее 6 нед. Не исключаются больные с двумя клиническими диагнозами. Чувствительность критериев составляет 91,2%, а специфичность — 89,3%.
Поскольку фармакотерапия РА более эффективна на ранних стадиях, его диагностика, как и других хронических заболеваний (сахарный диабет, артериальная гипертензия, ИБС и др.), должна осуществляться как можно раньше. РА следует заподозрить у больных с припухлостью суставов (особенно характерно симметричное поражение мелких суставов кистей и стоп), болями в суставах воспалительного характера, общими симптомами (лихорадка, похудание), увеличением СОЭ (более 25 мм/ч), титров РФ (более 1:40).
Диагностические критерии (АСR, 2002)
Диагноз = 4 из 7 критериев:
- Утренняя скованность суставов >1 часа
- Припухание 3 суставных зон и более, наблюдавшееся врачем
- Припухание суставов кисти
- Симметричность припухания
- Ревматоидные узелки
- РФ в плазме крови
- R изменения (эрозии, отчетливый остеопороз)
Критерии 1-4 должны присутствовать не менее 6 недель)
Критерии ранней диагностики РА (по Emeri)
- Три и более воспаленных сустава
- Поражение пястно-фаланговых и плюснефаланговых суставов: положительный тест поперечного «сжатия»
- Утренняя скованность более 30 мин.
Критерии ремиссии (АRA,1981)
Полное отсутствие следующих признаков:
- Симптомы активного воспаления суставов
- Утренняя скованность
- Усталость
- Синовит при осмотре сустава
- Прогрессирование рентгенологических изменений
- Повышение СОЭ или С-реактивного белка
9. Лечение
Лечение больных РА следует начинать в специализированном ревматологическом стационаре.
Общие рекомендации
- Обсудить с пациентами план лечения, объяснить характер болезни.
- Оценить домашнюю и рабочую обстановку, при необходимости рекомендовать смену профессии и стиля жизни (избегать избыточной нагрузки на поражённые суставы и др.).
- Обеспечить полноценную разгрузку и защиту поражённых суставов (ортопедические приспособления), наметить программу физиотерапии и лечебной физкультуры.
- При необходимости назначить терапию по поводу язвенной болезни, проводить профилактику и лечение остеопороза, контролировать АД и интеркуррентные инфекции.
Нестероидные противовоспалительные средства
НПВС — класс лекарственных средств, обладающих противовоспалительной, анальгетической и жаропонижающей активностью.
Классификация НПВС по селективности (по J. Floridi)
Селективные ингибиторы ЦОГ-1- низкие дозы ацетилсалициловой кислоты
Неселективные ингибиторы ЦОГ-1 и ЦОГ-2 — большинство НПВС, в том числе диклофенак натрия, кетопрофен, декскетопрофен и т.д.
Преимущественные ингибиторы ЦОГ-2 — мелоксикам, нимесулид
Специфические ингибиторы ЦОГ-2 – целекоксиб
Основной механизм действия НПВС — ингибирование синтеза циклооксигеназы (ЦОГ) — ключевого фермента метаболизма арахидоновой кислоты (предшест-венника ПГ). Установлено существование двух изоформ ЦОГ: структурного изофермента (ЦОГ-1), регулирующего продукцию ПГ, участвующих в обеспечении нормальной (физиологической) функциональной активности клеток, и «индуцируемого» изофермента (ЦОГ-2), экспрессия которого регулируется провоспалительными цитокинами, принимающими участие в развитии иммунного ответа и воспаления. Противовоспалительное, анальгетическое и жаропонижающее действие НПВС связано с их способностью ингибировать ЦОГ-2, в то время как наиболее часто встречающиеся побочные эффекты (поражение ЖКТ, почек, нарушение агрегации тромбоцитов) — с подавлением активности ЦОГ-1. НПВС, селективно (нимесулид, мелоксикам) или специфически (целекоксиб), ингибирующие ЦОГ-2, обладают такой же эффективностью, как и «стандартные» НПВС, но меньшей гастротоксичностью. В то же время у коксибов выявлен повышенный риск тромбозов, включая инфаркты миокарда и инсульты.
Применение НПВС — основной метод симптоматического лечения РА, направ-ленный на уменьшение боли и воспаления в суставах. К недостаткам НПВС относят то, что эти препараты недостаточно эффективно контролируют клинические проявления артрита, не влияют на прогрессирование повреждения суставов и вызывают побочные эффекты, особенно у лиц пожилого возраста. В процессе лечения очень большое значение имеет контроль побочных реакций (язвенно-некротическое поражение ЖКТ, нарушения функции почек и др.). При выборе НПВС необходимо учитывать эффективность и переносимость препарата, возраст больных, сопутствующую патологию, приём других препаратов и прошлый опыт больного.
Основные побочные эффекты НПВС
- Органы пищеварения: НПВС-гастропатия, эзофагопатия, энтеропатия, колопатия, гепатопатия, функциональная диспепсия.
- Кардиологические: артериальная гипертензия, прогрессирование хронической сердечной недостаточности, периферические отеки.
- Почечные: снижение клубочковой фильтрации, интерстициальный нефрит
- Тромбоцитарные: нарушение агрегации, повышение риска кровотечений.
- Бронхолегочные: аспириновая бронхиальная астма
- Костно-суставные: дегенеративное действие на хрящ, прогрессирование остеопороза.
- Неврологические: нарушение функции ЦНС, включая забывчивость, неспособность сосредоточиться, бессонницу, паранойю, депрессию.
При приеме НПВС для контроля побочного действия необходим динамический расспрос: наличие мелены или крови в стуле, диспепсия, боли в животе, отеки, затрудненное дыхание, уровень АД, изменение симптомов в сердечной недостаточности по В.Ю. Марееву, забор кала на скрытую кровь, биохимия крови (креатинин, билирубин, АЛТ, АСТ), ФГДС.
Для профилактики гастропатии у лиц с факторами риска применяют ингибиторы протонной помпы: омепразол 20-40 мг, ланзопразол 30-60 мг/сут, эзомепразол 20-40 мг.
Глюкокортикоиды
Низкие дозы ГКС (менее 10 мг/сут) используют в качестве так называемой «бридж»-терапии (от англ. bridge — мост) до того момента, когда начнут действовать базисные противоревматические препараты, особенно у тех больных, у которых симптомы не контролируются НПВС. Нередко лечение низкими дозами ГКС позволяет адекватно контролировать воспаление при РА, не уступая в этом отношении базисным противоревматическим препаратам, вызывает меньше побочных эффектов, снижает скорость рентгенологического прогрессирования раннего активного РА (особенно при сочетании с метотрексатом). Однако длительное лечение ГКС нежелательно, так как приводит к осложнениям, в частности остеопорозу, поэтому желательно сразу назначать средства для коррекции данного состояния – препараты кальция, витамина D, бисфосфонатов, кальцитонина.
Пульс-терапия ГКС — быстрое (в течение 30-60 мин) в/в введение больших доз ГКС Пульс-терапия ГКС (метилпреднизолон, дексаметазон) позволяет достигнуть быстрого (в течение 24 ч), но кратковременного (3-12 нед) подавления активности воспалительного процесса даже у больных, резистентных к предшествующей терапии. Однако влияние пульс-терапии на рентгенологическое прогрессирование поражения суставов не доказано.
Местная терапия ГКС
Местная терапия ГКС имеет вспомогательное значение. Её цель — подавление активного синовита в начале болезни и его обострений в одном или нескольких суставах, улучшение функции суставов. Однако ГКС оказывают влияние только на локальное воспаление (в то время как воспаление при РА носит системный характер) и вызывают только временное улучшение. ГКС, применяемые для местной терапии, подразделяют на препараты короткого (гидрокортизон) и пролонгированного действия. Последние, в свою очередь, включают препараты средней продолжительности действия (метилпреднизолон) и длительно действующие (бетаметазона дипропионат). Гидрокортизон используют главным образом для купирования синовита мелких суставов кистей и стоп, тендосиновитов и воспаления периартикулярных мягких тканей, а при воспалении крупных суставов, как правило, применяют пролонгированные препараты. Наиболее эффективны пролонгированные ГКС.
Базисная терапия
Современные требования к базисной терапии предусматривают выполнение следующих принципов:
Базисные препараты необходимо назначать не позднее 3 месяцев с момента установления диагноза всем больным с активным РА, у которых, несмотря на лечение НПВП, прогрессирует или стойко сохраняется активный воспалительный процесс в суставах.
Неэффективные на протяжении 1,5-3 мес. базисные препараты должны быть заменены или использована их комбинация и/или назначены низкие дозы ГКС. 6 месяцев – критический срок, не позднее которого должна быть подобрана действенная базисная терапия.
Эффективные базисные препараты не отменяются, а используются в поддерживающей дозе неопределенно долго (до утраты эффективности или развития побочных действий). — Лучшим препаратом для начала базисной терапии при тяжелом течении РА, РФ- позитивности, наличии внесуставных проявлений является метотрексат. Решение о его неэффективности может быть принято только после ступенчатого повышения дозы до 20- 30 мг в неделю.
Комбинации базисных препаратов (метотрексат+плаквенил; метотрексат+сульфасалазин; метотрексат+сульфасалазин+плаквенил; метотрексат+лефлюномид; препараты золота+плаквенил) используются при агрессивном течении РА, недостаточном эффекте (частичной реакции или рефрактерности) отдельных базисных препаратов.
Слабые (делагил/плаквенил, пероральные препараты золота) и медленно действующие (делагил/плаквенил, парентеральные препараты золота) базисные препараты могут применяться в качестве монотерапии (без комбинации с метотрексатом, сульфасалазином, или ГКС-”мостика”) только при мало прогрессирующем течении РА, I степени активности.
Таблица. Характеристика основных базисных препаратов для лечения РА.
| Препарат | Время развития клинического эффекта | Обычная поддерживающая доза |
| Плаквенил | 2-6 месяцев | 0,2 г х 2 р./д. |
| Сульфасалазин | 1-2 месяца | 1 г х 2р./д. |
| Метотрексат | 1-2 месяца | 7,5 — 20 мг/нед. |
| Лефлуномид | 1 месяц | 10 — 20 мг/д. |
| Золото в/м | 3-6 месяцев | 25 — 50 мг в/м каждые 2-4 недели |
| Золото per os | 4-6 месяцев | 3 мг х 2 р./д. |
| Азатиоприн | 2-3 месяца | 50 мг х 1-3 р./д. |
| D-пеницилламин | 3-6 месяцев | 0,25 г х 1-3 р./д. |
| Циклоспорин | 2-4 месяца | 2,5-4 мг/кг/д. |
| Инфликсимаб | 1 месяц | 3 мг/кг в течение 2 часов, через 2 и 6 недель в той же дозе, затем кадые 8 недель в той же дозе. |
| Циклофосфамид | 2-3 месяца | 50-100 мг/сут |
У больных с низкой активностью РА без факторов риска неблагоприятного прогноза целесообразно назначение наиболее безопасных препаратов, к которым относят гидроксихлорохин (плаквенил) и сульфасалазин. Назначение сульфасалазина особенно показано больным с серонегативным РА, который иногда трудно дифференцировать от серонегативных спондилоартропатий.
Для больных с умеренной (или высокой) активностью, имеющих факторы неблагоприятного прогноза, препарат выбора — метотрексат. В низких дозах его противовоспалительное действие связано с увеличением местной продукции аденозина в очаге воспаления. В свою очередь, аденозин обладает мощной естественной противовоспалительной и иммуномодулирующей активностью. Преимуществом метотрексата (по сравнению с другими базисными препа-ратами) являются относительно быстрое развитие противовоспалительного действия и низкая токсичность при длительном применении. Применение метотрексата позволяет существенно улучшить прогноз у больных РА. Следует иметь в виду, что лечение метотрексатом несовместимо с употреблением алкоголя. Достаточно высокой эффективностью обладают препараты золота, пеницилламин и азатиоприн, но они чаще, чем метотрексат, вызывают побочные эффекты, при которых необходимо прервать лечение. Циклоспорин также зарекомендовал себя как эффективный препарат для лечения больных РА, особенно на ранних стадиях болезни.
Учитывая фундаментальное значение ФНО-альфа в иммунопатогенезе РА, в последние годы для лечения этого заболевания применяют несколько новых биологических препаратов, специфически ингибирующих синтез ФНО-альфа. К ним относят моноклональные AT к ФНО-альфа: химерные (инфликсимаб). На фоне лечения ингибиторами ФНО-альфа удаётся добиться выраженного клинического улучшения даже у пациентов, резистентных к другим базисным противоревматическим препаратам, и замедлить рентгенологическое прогрессирование суставной деструкции. Особенно перспективно комбинированное лечение моноклональными AT к ФНО-альфа в сочетании с метотрексатом.
Лечение РА с системными проявлениями
Наиболее эффективный метод лечения РА — интермиттирующая пульс-терапия циклофосфамидом (2-5 мг/кг/сут) и метилпреднизолоном (1 г/сут) каждые 2 нед в течение 6 нед, с последующим удлинением интервала между введениями. Иногда назначают хлорбутин коротким курсом, однако длительное лечение не рекомендуют из-за риска развития злокачественных новообразований. Активная терапия позволяет довольно быстро (в течение 3-6 мес) достигнуть ремиссии при ревматоидном васкулите. Для поддержания ремиссии используют азатиоприн. При криоглобулинемии и тяжёлых проявлениях васкулита целесообразно проведение плазмафереза.
Реабилитация
Для профилактики деформации суставов следует рекомендовать изменение стереотипа двигательной активности. Например, для профилактики ульнарной девиации кисть должна выполнять не локтевое, а лучевое сгибание: открывать кран и поворачивать ключ в замке не правой, а левой рукой и др. Важный компонент лечения РА — лечебная физкультура. При небольшой или умеренной активности показаны различные методы физиотерапии, особенно лазерное облучение поражённых суставов. Санаторно-курортное лечение показано только больным с минимальной активностью РА или в стадии ремиссии.
Ортопедическое лечение
В качестве ортопедического пособия применяют особые ортопедические приспособления из термопластика, надеваемые на время сна, удерживающие сустав в правильном положении. Широко используют эндопротезирование тазобедренных и коленных суставов и хирургическое лечение деформаций кистей и стоп.
9. Прогноз
К факторам, связанным с агрессивным течением РА и неблагоприятным прогнозом, относят:
- серопозитивность по РФ в дебюте болезни
- женский пол
- молодой возраст в начале болезни
- внесуставные (системные) проявления
- высокую лабораторную активность (увеличение СОЭ и СРВ, тромбоцитоз)
- носительство HLA-DR4
- раннее появление и быстрое прогрессирование эрозий в суставах
- раннее нарушение функции суставов
- низкий социальный статус пациентов
Ожидаемая продолжительность жизни у больных РА снижена на 3 года у женщин и на 7 лет у мужчин. Однако, поскольку причины смерти у больных РА не отличаются от таковых в общей популяции, этот диагноз в большинстве случаев не фигурирует среди причин смерти. Смертность у больных РА выше, чем в общей популяции, от инфекций, поражений почек и ЖКТ, респираторных заболеваний, в то время как смертность от злокачественных новообразований, несмотря на лечение цитотоксическими препаратами, ниже. Последнее может быть связано с противоопухолевым действием НПВС, обладающих антипро-лиферативной активностью за счёт ингибирования ЦОГ-2. Полагают, что одной из причин снижения продолжительности жизни у больных РА выступает субклинически текущий васкулит, создающий предпосылки для раннего развития атеросклеротического поражения сосудов. Однако смертность от заболеваний сердечно-сосудистой системы у больных РА такая же, как и в общей популяции (примерно 40%). Особенно неблагоприятен прогноз при ревматоидном васкулите: 3–5–летняя выживаемость больных колеблется от 28 до 40%, несмотря на использование интенсивной терапии.
Литература
- Избранные лекции по клинической ревматологии. М.: Медицина; 2001. 272 с.
- Каратеев Д.Е., Олюнин Ю.А. О классификации ревматоидного артрита. Научно-практическая ревматология 2008;1:5-16.
- Классификация и критерии диагностики ревматологических заболеваний. Под ред. Ю.А. Горяева. Иркутск; 2006. 84 с.
- Клинические рекомендации. Ревматология. М.: Гоэтар-Медиа, 2006; 264 с.
- Насонов Е.Л. Клинические рекомендации. Ревматология. М.:Гэотар-Медицина; 2006. 288 с.
- Окороков А.Н., Базенко Н.П. Ревматоидный артрит. М: Мед. лит.; 2003. 176 с.
- Рациональная фармакотерапия ревматических заболеваний. Под ред. В.А. Насоновой, Е.Л. Насонова. М.: Литера; 2003. 506 с.
- Сорока Н.Ф., Ягур В.В. Ревматоидный артрит; проблемы диагноза и лечения. Минск: Беларусь; 2000. 190 с.
- BSR guidelines on standards of care for persons with rheumatoid arthritis. Rheumatology 2005;44:553-6.
- Guidelines for the Management of Rheumatoid Arthritis. 2002 Update. Arthritis & Rheumatism 2002;46 (2):328-346.